
| A. | 64g/mol | B. | 32g/mol | C. | 32g | D. | 16g |
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:解答题
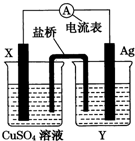 依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池,如图所示.请回答下列问题.
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池,如图所示.请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=110.5 kJ•mol-1 | |
| B. | C(s)+O2(g)═CO2(g)△H=-393.5 kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2和O2反应生成水 | B. | 锌片投入稀硫酸中 | ||
| C. | 木炭在高温下与CO2反应生成CO | D. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 除去Cu(NO3)2溶液中混有的AgNO3:加入适量铜粉 | |
| B. | 分离溴和CCl4的混合物:分液 | |
| C. | 区分NaCl和KCl溶液:焰色反应 | |
| D. | 检验某未知溶液中的SO42-:加入稀硝酸酸化的BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
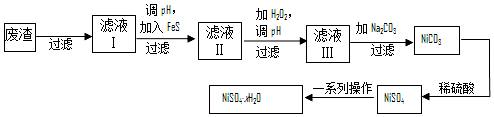
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
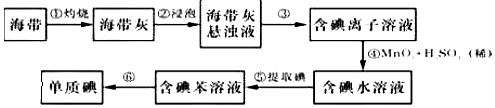
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 CH3COOH溶液与0.1 mol•L-1NaOH溶液等体积混合 | |
| B. | 向40mL0.2 mol•L-1的NaOH溶液中通入67.2mLCO2(标况) | |
| C. | 在100mL1 mol•L-1NH4Cl溶液中,投入3.9gNa2O2 | |
| D. | 在20mL0.01 mol•L-1Ma(HCO3)2溶液中,投入0.2g Ma(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Ag+、NO3-、Cl- | B. | NH4+、Ba2+、Cl-、CO32- | ||
| C. | H+、Ca2+、CO32-、NO3- | D. | Na+、Al3+、SO42-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com