
 ,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.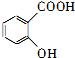 .
. (其中两种).
(其中两种). 为主要原料制备
为主要原料制备 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{△}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{△}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$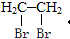
分析 C遇FeCl3水溶液显紫色,与NaHCO2溶液反应有CO2产生,说明C中含有酚羟基和羧基,结合A的结构简式、B的分子式、C的分子式知,X前边的属于B中部分,所以B的结构简式为: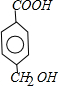 ,根据B的结构简式确定其具有的性质;
,根据B的结构简式确定其具有的性质;
C中含有羧基和酚羟基,根据RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH知,C中的羧基被含有生成醇羟基,所以D中含有酚羟基和醇羟基,D中醇羟基和氢溴酸发生取代反应生成E,E中含有酚羟基和溴原子,根据R-Br$→_{②H+}^{①NaCN}$R-COOH知,E中溴原子被取代生成羧基,在浓硫酸作催化剂、加热条件下,F发生酯化反应生成G,分子式为C8H6O2,分子内含有五元环,所以F发生分子内酯化反应生成G,则F的结构简式为: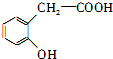 ,G的结构简式为:
,G的结构简式为: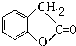 ,C的结构简式为:
,C的结构简式为: ,D的结构简式为:
,D的结构简式为: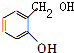 ,E的结构简式为:
,E的结构简式为: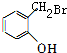 ,A的结构简式为:
,A的结构简式为: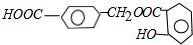 ,根据物质的结构和性质解答.
,根据物质的结构和性质解答.
解答 解:C遇FeCl3水溶液显紫色,与NaHCO2溶液反应有CO2产生,说明C中含有酚羟基和羧基,结合A的结构简式、B的分子式、C的分子式知,X前边的属于B中部分,所以B的结构简式为: ,根据B的结构简式确定其具有的性质;
,根据B的结构简式确定其具有的性质;
C中含有羧基和酚羟基,根据RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH知,C中的羧基被含有生成醇羟基,所以D中含有酚羟基和醇羟基,D中醇羟基和氢溴酸发生取代反应生成E,E中含有酚羟基和溴原子,根据R-Br$→_{②H+}^{①NaCN}$R-COOH知,E中溴原子被取代生成羧基,在浓硫酸作催化剂、加热条件下,F发生酯化反应生成G,分子式为C8H6O2,分子内含有五元环,所以F发生分子内酯化反应生成G,则F的结构简式为: ,G的结构简式为:
,G的结构简式为: ,C的结构简式为:
,C的结构简式为: ,D的结构简式为:
,D的结构简式为: ,E的结构简式为:
,E的结构简式为: ,A的结构简式为:
,A的结构简式为: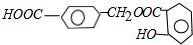 ,
,
(1)A的结构简式知,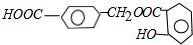 ,所以A中含有酯基、酚羟基和羧基,
,所以A中含有酯基、酚羟基和羧基,
故答案为:酯基;
(2)B的结构简式为: ,所以B能发生取代反应、加成反应和缩聚反应,故选abc;
,所以B能发生取代反应、加成反应和缩聚反应,故选abc;
(3)①C的结构简式为: ,
,
故答案为: ;
;
②符合条件的E的同分异构体为: ,
,
故答案为: (其中两种);
(其中两种);
(4)苯乙烯和溴发生加成反应生成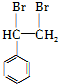 ,
,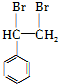 和氰化钠反应,然后酸化生成
和氰化钠反应,然后酸化生成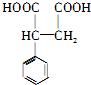 ,
, 被还原生成
被还原生成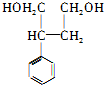 ,
, 和
和 发生酯化反应生成
发生酯化反应生成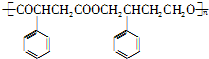 ,所以其合成路线为:
,所以其合成路线为: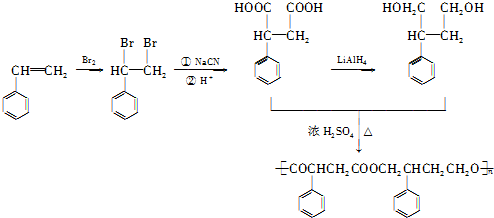 ,
,
故答案为: .
.
点评 本题考查有机物的推断及合成,明确有机物的官能团及性质是解本题关键,采用正、逆推相结合的方法进行分析,难点是设计合成路线,要求学生不仅掌握有机物的结构、性质还要掌握其反应条件,明确有机物的断键方式,难度较大.


科目:高中化学 来源: 题型:解答题
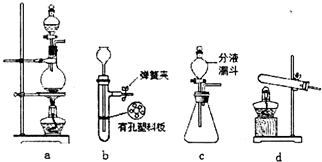 硫化亚铁是一种黑色块状固体,常温下难溶于水,易溶于酸而生成能溶于水的硫化氢气体.硫化亚铁在空气中煅烧时生成二氧化硫气体和烧渣.
硫化亚铁是一种黑色块状固体,常温下难溶于水,易溶于酸而生成能溶于水的硫化氢气体.硫化亚铁在空气中煅烧时生成二氧化硫气体和烧渣.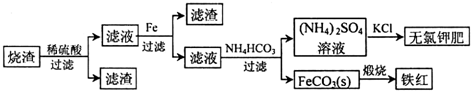
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
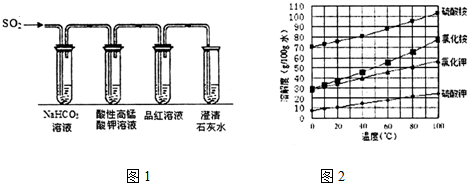
 ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙和盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 向氢氧化钡溶液中加硫酸溶液:Ba2++SO42-═BaSO4↓ | |
| C. | 向稀盐酸溶液中加铁:3Fe+6H+═3Fe3++3H2↑ | |
| D. | 向硝酸银溶液中加盐酸:Ag++Cl-═AgCl↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16.51 g | B. | 23.82 g | C. | 24.84 g | D. | 17.02 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
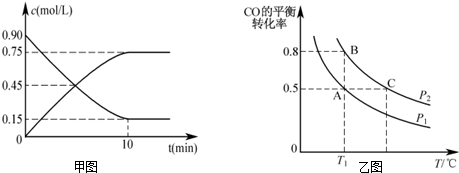
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
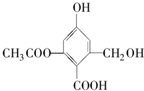
| A. | X的化学式为C10H10O6 | |
| B. | X在一定条件下能与FeCl3溶液发生显色反应 | |
| C. | 1mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3mol、5mol、1mol | |
| D. | X既可以和乙醇又可以和乙酸发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
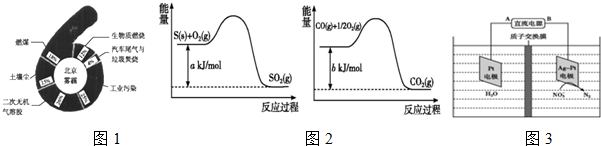
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com