
2.7 g
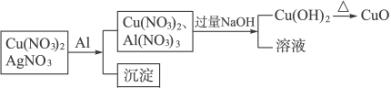
解析:本题中涉及的化学反应有:
Al+3AgNO3====3Ag+Al(NO3)3
2Al+3Cu(NO3)2====2Al(NO3)3+3Cu(可能)
Al(NO3)3+4NaOH====NaAlO3+3NaNO3+2H2O
Cu(NO3)2+2NaOH====Cu(OH)2↓+2NaNO3
Cu(OH)2![]() CuO+H2O
CuO+H2O
可发现以下关系:
因此,本题求解中可抓住加入铝经充分反应后的溶液为Al(NO3)3和Cu(NO3)2的混合溶液这一关系,并利用Al3+和Cu2+所带正电荷总数等于![]() 所带负电荷总数以及Cu、Al、
所带负电荷总数以及Cu、Al、![]() 守恒等守恒关系列式。
守恒等守恒关系列式。
依题意和有关守恒关系有:
3n(Al)+2n(CuO)====n(![]() )
)
即:n(Al)=![]() =0.1 mol
=0.1 mol
m(Al)=0.1 mol×27 g·mol-1=2.7 g


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
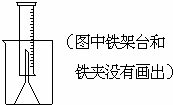 测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:中学化学实验常用仪器.800毫升烧杯.100毫升量筒.短颈玻璃漏斗.铜网.铝锌合金样品.浓盐酸(密度1.19克/毫升).水.按图示装置进行实验,回答下列问题.(设合金样品完全反应,产生的气体体积不超过100毫升)
测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:中学化学实验常用仪器.800毫升烧杯.100毫升量筒.短颈玻璃漏斗.铜网.铝锌合金样品.浓盐酸(密度1.19克/毫升).水.按图示装置进行实验,回答下列问题.(设合金样品完全反应,产生的气体体积不超过100毫升)查看答案和解析>>
科目:高中化学 来源:101网校同步练习 高二化学 山东科学技术出版社 鲁教版 题型:058
溴乙烷是重要的化工原料,实验室制取溴乙烷(沸点为38.4℃)的原理及步骤如下:
(1)反应原理
C2H5OH+NaBr+H2SO4![]() NaHSO4+C2H5Br+H2O
NaHSO4+C2H5Br+H2O
(2)主要反应装置如图:
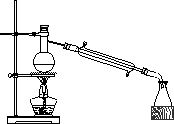
(3)操作步骤
①在100 mL的圆底烧瓶中加入10 mL 95%的乙醇.28 mL 78%的硫酸,然后加入研细的13 g溴化钠.
②加入几块碎瓷片,小心摇动烧瓶使其混合均匀.将烧瓶与直形冷凝管相连,冷凝管下端连接尾接管.
③小心加热,使其充分反应,再进行蒸馏,直到无溴乙烷流出为止.
④再将锥形瓶中的液体冷却后倒入亚硫酸钠溶液中洗涤分液.
试回答下列问题:
(1)本实验中用的是78%的硫酸,为何不用浓硫酸?________.
(2)亚硫酸钠溶液的作用是________.
(3)该实验中会发生许多生成有机物的副反应,写出有关化学方程式________(举两例)
(4)本实验只收集到5 mL溴乙烷,比理想产量约10 mL少,原因是溴乙烷易挥发,为了减少其损失,你认为可采取什么措施?________.
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下,足量MnO2氧化了100 mL的浓盐酸,生成Cl2体积为3.36 L,该盐酸物质的量浓度是()
A.3 mol·L-1 B.0.3 mol·L-1
C.6 mol·L-1 D.0.6 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
若配制500 mL 0.2 mol/L的稀硫酸:
(1)需要量取质量分数为98%的硫酸(密度为1.84 g·mL-1)_____________mL。
(2)下面是某学生的操作过程:
a.检查容量瓶是否漏水;b.用100 mL的量筒量取浓硫酸;
c.将浓硫酸倒入另一个盛有适量蒸馏水的量筒中稀释,并冷却到室温;
d.用玻璃棒引流,将稀释后的硫酸倒入500 mL的容量瓶;
e.轻轻摇动容量瓶,使瓶内液体混合均匀,再向容量瓶中加水至离刻度线1 cm~2 cm;
f.用胶头滴管加水至凹液面底部与刻度线相切,摇匀;
g.在容量瓶上贴上标签待用。
按照通常的配制要求,指出其中缺少或操作的错误,并补充或改正(有几项填几项,若空格不够可以补加)。
①________________________________________________________;
②________________________________________________________;
③________________________________________________________;
④________________________________________________________;
⑤________________________________________________________。
(3)任何实验都有误差,在你改正后的操作中,产生误差的原因还有_________________。(4)本实验最浪费时间的步骤是将稀释后的硫酸冷却到室温,为了节约时间,简便易行的加快稀硫酸冷却的方法是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)实验室用98%的浓硫酸(其密度为1.84 g/ml)配制100 mL
1.0 mol·L-1稀硫酸。
(1)需用10 mL的量筒量取浓硫酸的体积为 mL。
(2)实验时选用的仪器有10 mL量筒、烧杯、玻璃棒、 、 。
(3)配制过程中,下列情况会使配制结果偏低的是(填序号) 。
A.用量筒量取浓硫酸时,仰视量筒的刻度
B.转移液体到容量瓶中时,未洗涤烧杯就定容
C.往容量瓶转移时,有少量液体溅出
D.容量瓶使用时未干燥
E.定容时俯视刻度线观察液面
(4)在容量瓶使用方法中,下列操作正确的是(填序号) 。
A.容量瓶用蒸馏水洗净后,再用待配液润洗
B.使用容量瓶前检查它是否漏水
C.将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.将准确量取的18.4mol·L-1的硫酸,注入已盛有30mL水的100 mL的容量瓶中,加水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com