
(18分)(1)在实验室制取蒸馏水的装置中,温度计的水银球应位于 ;烧瓶中应放几粒沸石(或碎瓷片),其作用是 ;冷凝管中冷凝水的流向应当是 (流向用上口、下口、谁为进水口,谁为出水口表示)。
(2)实验室欲配制0.5 mol·L-1的NaOH溶液500mL,有以下仪器:
①烧杯 ②100 mL量筒 ③1000 mL 容量瓶 ④500mL 容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码)
a:配制时,必须使用的仪器有 (填代号),还缺少的仪器是 ,该实验中两次用到玻璃棒,其作用分别是 、 。
b:配制时,一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容⑧冷却,其正确的操作顺序是 。
c:在配制NaOH溶液时,下列操作会导致结果偏低的是
(1)用拖盘天平称量时砝码放在左盘(2)溶解NaOH固体后没有冷却至室温就向容量瓶转移溶液
(3)将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外(4)定容时俯视刻度线(5)定容时仰视刻度线
(6)干净的容量瓶未经干燥就用于配制溶液
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
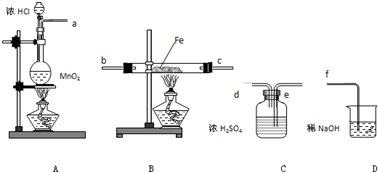
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
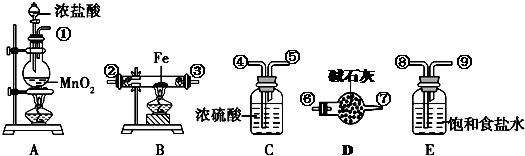
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com