
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极极板,通过导线与直流电源相连。下列说法不正确的是 ( )
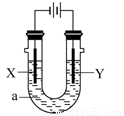
A.若电镀铜,则Y为铜电极,电解液a可以是硫酸铜或氯化铜溶液
B.若X为铁电极、Y为石墨电极,电解饱和氯化钠溶液一段时间,在两极分别滴加酚酞,X极变红色
C.若用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.1mol的 氢氧化铜溶解,刚好恢复到通电前的浓度,则电解过程中转移的电子为0.2mol
D.若X、Y为铂电极,a溶液为250mL CuSO4和KNO3的混合液,经过一段时间后,两极均得到标准状况下5.6L气体,则原混合液中CuSO4的物质的量浓度为1mol·L-1
C
【解析】
试题分析:A、根据电镀池的构成:镀层材料作阳极,镀件作阴极电解质溶液为含有镀层金属阳离子的盐溶液来判断,正确;B、根据电解饱和氯化钠溶液的原理判断,正确;C、电解硫酸铜溶液的反应方程式为: 2CuSO4+2H2O 2Cu+ 2H2SO4+O2↑ 从上述方程式可以看出,电解硫酸铜过程中,只析出铜和释放出氧气。因此电解后加入CuO就可以使溶液复原。本题加入Cu(OH)2后溶液复原,说明电解过程中还有水被电解(因为硫酸铜被电解完全)。0.1molCu(OH)2可以可以看作是0.1mol的CuO和0.1mol H2O,因此电解过程中有0.1mol的硫酸铜和0.1mol的水被电解,转移电子的物质的量是0.4mol,错误;D、电解硫酸铜和硝酸钾混合溶液,阳极上氢氧根离子放电生成氧气,阴极上先铜离子放电析出铜,当铜完全析出时,氢离子放电析出氢气,根据转移电子守恒计算析出铜的物质的量,再结合物质的量浓度公式计算硫酸铜溶液浓度。
2Cu+ 2H2SO4+O2↑ 从上述方程式可以看出,电解硫酸铜过程中,只析出铜和释放出氧气。因此电解后加入CuO就可以使溶液复原。本题加入Cu(OH)2后溶液复原,说明电解过程中还有水被电解(因为硫酸铜被电解完全)。0.1molCu(OH)2可以可以看作是0.1mol的CuO和0.1mol H2O,因此电解过程中有0.1mol的硫酸铜和0.1mol的水被电解,转移电子的物质的量是0.4mol,错误;D、电解硫酸铜和硝酸钾混合溶液,阳极上氢氧根离子放电生成氧气,阴极上先铜离子放电析出铜,当铜完全析出时,氢离子放电析出氢气,根据转移电子守恒计算析出铜的物质的量,再结合物质的量浓度公式计算硫酸铜溶液浓度。
考点:考查电解原理的应用。


科目:高中化学 来源: 题型:
 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | Fe(NO3)3 |
| D | 铁 | 银 | AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 (I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.
(I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.查看答案和解析>>
科目:高中化学 来源: 题型:
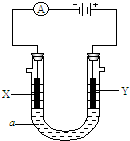
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com