
 为原料,按以下步骤从合成
为原料,按以下步骤从合成  (部分试剂和反应条件已略去).
(部分试剂和反应条件已略去).
 .
. $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O. 有多种同分异构体,其中既能发生水解反应,又能发生银镜反应的有机物共有8种.
有多种同分异构体,其中既能发生水解反应,又能发生银镜反应的有机物共有8种. 分析  与氢气发生加成反应可生成A为
与氢气发生加成反应可生成A为 ,环己醇在浓硫酸作用下发生消去反应生成B为
,环己醇在浓硫酸作用下发生消去反应生成B为 ,环己烯与溴发生加成反应生成C为
,环己烯与溴发生加成反应生成C为 ,C在氢氧化钠醇溶液、加热条件下发生消去反应生成D(
,C在氢氧化钠醇溶液、加热条件下发生消去反应生成D( ),
), 与溴发生1,4-加成生成E为
与溴发生1,4-加成生成E为 ,
, 与氢气发生加成反应生成F为
与氢气发生加成反应生成F为 ,F在氢氧化钠水溶液、加热条件下发生水解反应生成
,F在氢氧化钠水溶液、加热条件下发生水解反应生成 ,以此来解答.
,以此来解答.
解答 解:(1)C为 ,C的名称是1,2-二溴环己烷,D的结构简式是
,C的名称是1,2-二溴环己烷,D的结构简式是 ,故答案为:1,2-二溴环己烷;
,故答案为:1,2-二溴环己烷; ;
;
(2)步骤⑦的反应类型是取代反应或水解反应,反应条件是NaOH水溶液、加热,故答案为:取代反应或水解反应;NaOH水溶液、加热;
(3)不考虑反应条件,步骤⑤通过加成反应得到的产物E, 可与溴1:1加成有2种产物(1,2加成方式或1,4加成方式),或生成与溴1:2加成有1种产物,则可能有3种,故答案为:3;
可与溴1:1加成有2种产物(1,2加成方式或1,4加成方式),或生成与溴1:2加成有1种产物,则可能有3种,故答案为:3;
(4)步骤②“A→B”的化学方程式为 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O,故答案为:
+H2O,故答案为: $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O;
+H2O;
(5) 有多种同分异构体,其中既能发生水解反应,又能发生银镜反应,应为甲酸戊酯,-C5H11有8种,则有机物共有8种,故答案为:8.
有多种同分异构体,其中既能发生水解反应,又能发生银镜反应,应为甲酸戊酯,-C5H11有8种,则有机物共有8种,故答案为:8.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团的变化、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯 | |
| B. | 苯乙烯在合适条件下催化加氢可生成乙基环己烷 | |
| C. | 乙醇可被重铬酸钾氧化成乙酸,溶液由橙色变成绿色 | |
| D. | 甲苯与氯气在光照下反应主要生成2,4二氯甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol葡萄糖能水解生成2molCH3CH2OH和2molCO2 | |
| B. | 在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀 | |
| C. | 欲检验蔗糖水解产物是否具有还原性,可向水解后的溶液中直接加入新制的Cu(OH)2并加热 | |
| D. | 油脂不是高分子化合物,1mol油脂完全水解生成1mol甘油和3mol高级脂肪酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 灼热的炭与CO2反应 | ||
| C. | 铝与稀盐酸 | D. | 铝粉与氧化铁粉末反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和镁分别与冷水反应,判断金属性强弱 | |
| B. | 在MgCl2与AlCl3溶液中分别加入过量氨水,判断Mg与Al的金属性强弱 | |
| C. | 硅酸钠溶液中通入CO2气体,判断碳与硅的非金属性强弱 | |
| D. | Br2与I2分别与足量H2反应,判断溴与碘的非金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
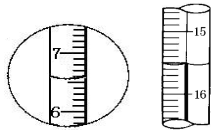
| A. | 左边是量筒读数6.5mL,右边是滴定管读数16.50mL | |
| B. | 左边是量筒读数7.5mL,右边是滴定管读数16.50mL | |
| C. | 左边是量筒读数6.5mL,右边是滴定管读数15.50mL | |
| D. | 左边是量简读数6.5mL,右边是滴定管读数16.50mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 91.8 | 96.5 | 98 | 99.8 | 9.8 | 96.4 | 93.0 | 89.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com