
| 0.3mol |
| 1mol/L |
|
|
| 0.34mol |
| 1mol/L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2012-2013学年黑龙江省鹤岗一中高二下学期期末考试化学试卷(带解析) 题型:填空题
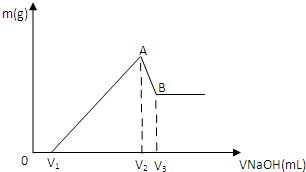
将0.1molMg、Al混合物溶于100mL4mol/L的盐酸中,然后再滴加1mol/L的NaOH溶液,在滴加NaOH溶液的过程中,沉淀质量m与NaOH溶液的体积V的变化如图所示。
(1)写出BC过程的离子反应方程式
(2)当V1=140mL时,混合物中n(Mg)=_____mol,V2=_____mL
(3)滴入的NaOH溶液_____mL时,溶液中的Mg2+和Al3+刚好沉淀完全。
(4)若混合物中Mg的物质的量分数为a,当滴入的NaOH溶液为450mL时,所得沉淀中无Al(OH)3,则a的取值范围是____________________
(5)当加入V2 mlNaOH溶液后过滤,向滤液中通入过量的CO2气体,能观察到的现象为 ,写出该过程反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2013届甘肃天水市一中高三第一次学段考试化学试卷(带解析) 题型:计算题
(8分) 将0.1molMg、Al混合物溶于100mL4mol/L的盐酸中,然后再滴加1mol/L的NaOH溶液,在滴加NaOH溶液的过程中,沉淀质量m与NaOH溶液的体积V的变化如图所示。
(1)当V1=140mL时,混合物中n(Mg)=_____mol,V2=_____mL
(2)滴入的NaOH溶液_____mL 时,溶液中的Mg2+和Al3+刚好沉淀完全。
(3)若混合物中Mg的物质的量分数为a,当滴入的NaOH溶液为450mL时,所得沉淀中无Al(OH)3,则a的取值范围是____________________
查看答案和解析>>
科目:高中化学 来源:2014届黑龙江省高二下学期期末考试化学试卷(解析版) 题型:填空题
将0.1molMg、Al混合物溶于100mL4mol/L的盐酸中,然后再滴加1mol/L的NaOH溶液,在滴加NaOH溶液的过程中,沉淀质量m与NaOH溶液的体积V的变化如图所示。
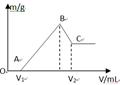
(1)写出BC过程的离子反应方程式
(2)当V1=140mL时,混合物中n(Mg)=_____mol,V2=_____mL
(3)滴入的NaOH溶液_____mL时,溶液中的Mg2+和Al3+刚好沉淀完全。
(4)若混合物中Mg的物质的量分数为a,当滴入的NaOH溶液为450mL时,所得沉淀中无Al(OH)3,则a的取值范围是____________________
(5)当加入V2 mlNaOH溶液后过滤,向滤液中通入过量的CO2气体,能观察到的现象为 ,写出该过程反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年吉林省长春市高一(上)期末化学试卷(解析版) 题型:解答题
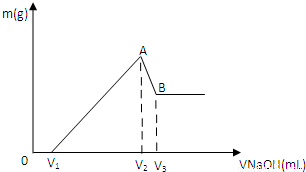
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com