
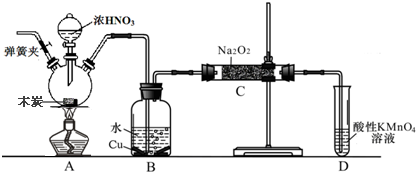
���� Aװ��ΪC��HNO3��Ũ����Ӧ���ɶ�����̼���������������������B����ˮ��Ӧ�����ᣬ������Cu��Ӧ����NO��Cװ�����Ʊ�NaNO2�����ڶ�����̼��ˮ������������Ʒ�Ӧ�ĵõ�̼���ơ��������ƣ�����Ҫ��Ҫ��ȥ������̼��������NO���壬������B��C֮�����ӳɷּ�ʯ�ҵ�װ�ã���Ӧ��ʼ��Ҫ�ž�װ���еĿ�������ֹ������NO�������������Ը��������Һ��Һ����δ��Ӧ��NO�����Է�ֹ��Ⱦ����������Ŀ��Ϣ�����������£�NO����MnO4-��Ӧ����NO3-��Mn2+��
��6�����ݷ���ʽ��C+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H2O��3NO2+H2O=2HNO3+NO��3Cu+8HNO3=3Cu��NO3��2+2NO��+4H2O��2NO+Na2O2�T2NaNO2���м��㣬����Bװ���еõ�NO��C���ʵ�����ϵ��
��� �⣺Aװ��ΪC��HNO3��Ũ����Ӧ���ɶ�����̼���������������������B����ˮ��Ӧ�����ᣬ������Cu��Ӧ����NO��Cװ�����Ʊ�NaNO2�����ڶ�����̼��ˮ������������Ʒ�Ӧ�ĵõ�̼���ơ��������ƣ�����Ҫ��Ҫ��ȥ������̼��������NO���壬������B��C֮�����ӳɷּ�ʯ�ҵ�װ�ã���Ӧ��ʼ��Ҫ�ž�װ���еĿ�������ֹ������NO�������������Ը��������Һ��Һ����δ��Ӧ��NO�����Է�ֹ��Ⱦ��������֤NO�Ļ�ԭ�ԣ�
��1����������ž���������ֹ���ɵ�NO��O2������
�ʴ�Ϊ���ž���������ֹ���ɵ�NO��O2������
��2������������B����ˮ��Ӧ�����ᣬ������Cu��Ӧ��������ͭ��NO���۲쵽������Ϊ������ɫ������ʧ��ͭƬ�ܽ⣬��Һ���������ܿ�����ɫ����ð����
�ʴ�Ϊ������ɫ������ʧ��ͭƬ�ܽ⣬��Һ���������ܿ�����ɫ����ð����
��3��C��HNO3��Ũ����Ӧ���ɶ�����̼�������������Ӧ����ʽΪ��C+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H2O��
�ʴ�Ϊ��C+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H2O��
��4������Ŀ��Ϣ�����������£�NO����MnO4-��Ӧ����NO3-��Mn2+����Ӧ���ӷ���ʽΪ��3MnO4-+5NO+4H+=3Mn2++5NO3-+2H2O��
�ʴ�Ϊ��3MnO4-+5NO+4H+=3Mn2++5NO3-+2H2O��
��5��������̼��ˮ������������Ʒ�Ӧ�ĵõ�̼���ơ��������ƣ�������B��C֮�����ӳɷּ�ʯ�ҵ�װ�ã����ճ�ȥ������̼��������NO���壬
�ʴ�Ϊ��NaOH����ʯ�ң�
��6��n��Na2O2��=$\frac{3.12g}{78g/mol}$=0.04mol������2NO+Na2O2=2NaNO2֪��0.04mol�������Ʒ�Ӧ��Ҫ0.08molNO����μӷ�Ӧ��̼Ϊ nmol������C+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H2O֪������4nmolNO2������3NO2+H2O=2HNO3+NO����֪4nmolNO2��ˮ��Ӧ����4nmol��$\frac{2}{3}$=$\frac{8}{3}$nmol�����$\frac{4}{3}$nmolNO���ٸ���3Cu+8HNO3=3Cu��NO3��2+2NO��+4H2O��֪��������ͭ��Ӧ���ɵ�NOΪ$\frac{8}{3}$nmol��$\frac{2}{3}$=$\frac{2}{3}$nmol������$\frac{4}{3}$nmol+$\frac{2}{3}$nmol=2nmol=0.08mol���ɵ�n=0.04mol������Ҫ̼������=12g/mol��0.04mol=0.48g��
�ʴ�Ϊ��0.48��
���� ���⿼�������Ʊ�ʵ�鷽������ƣ��漰��ԭ����װ�õķ������ۡ���Ϣ��ȡ��Ǩ�����á���ѧ����ȣ���6���м���Ϊ�״��㡢�ѵ㣬�ؼ��Ǹ��ݷ���ʽ����Bװ���еõ�NO��̼�����ʵ�����ϵ��


 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
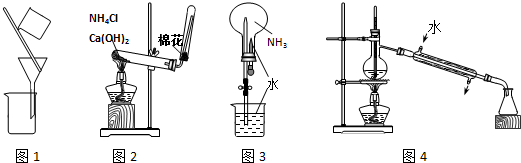
| A�� | ��ͼ1װ�÷����Ҵ������� | B�� | ��ͼ2װ����ȡ���� | ||
| C�� | ��ͼ3װ�ý��а�������Ȫʵ�� | D�� | ��ͼ4װ�ý���ʯ�͵ķ���ʵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
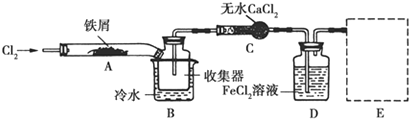
| A�� | ��Һ�д������棺Na+��Ba2+��Cl-��CO32- | |
| B�� | ��ɫ��Һ���ܴ������棺NH4+��Fe3+��SO42-��CI- | |
| C�� | �������������ᷴӦ�����ӷ���ʽ�ǣ�3H++Fe��OH��3�TFe3++3H2O | |
| D�� | ̼��������Һ���������Ʒ�Ӧ�����ӷ���ʽ�ǣ�HCO3-+OH-�TH2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
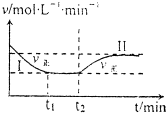 ��ijһ���º��ݵ��ܱ������з������·�Ӧ��3H2��g��+N2��g��?2NH3��g����H��O��t1ʱ�̵���ƽ�����t2ʱ�̸ı�ijһ�������䷴Ӧ������ͼ��ʾ������˵����ȷ���ǣ�������
��ijһ���º��ݵ��ܱ������з������·�Ӧ��3H2��g��+N2��g��?2NH3��g����H��O��t1ʱ�̵���ƽ�����t2ʱ�̸ı�ijһ�������䷴Ӧ������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | �������̴ﵽƽ��ʱ��ƽ�ⳣ����K��K�� | |
| B�� | �������̴ﵽƽ��ʱ��NH3������������� | |
| C�� | �������̴ﵽƽ��ı�־�������ܶȲ��ٷ����仯 | |
| D�� | t2ʱ�̸ı���������������ܱ������м�H2��N2����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
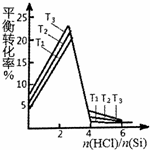 ������裨SiHCl3���������ྦྷ�����Ҫԭ�ϣ��ɴֹ����������ķ�Ӧ���£�
������裨SiHCl3���������ྦྷ�����Ҫԭ�ϣ��ɴֹ����������ķ�Ӧ���£�| ��Ӧ���Ȼ�ѧ����ʽ | ƽ�ⳣ����300�棩 | |
| ����Ӧ | Si��s��+3HCl��g��?SiHCl3��g��+H2��g����H=-210kJ•mol-1 | K1��mol•L-1��-1 |
| ����Ӧ | Si��s��+4HCl��g��?SiHCl4��g��+2H2��g����H=-240kJ•mol-1 | K2��mol•L-1��-1 |
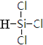 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| t/min | 0 | 2 | 4 | 7 | 9 |
| n��B��/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
| A�� | �����������䣬��ƽ����ϵ���ٳ���0.32molA���ٴﵽ��ƽ��ʱ��B��ת�������� | |
| B�� | �����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰ�ͣ��棩���ͣ����� | |
| C�� | �����������䣬��ʼʱ�������г���0.64molA��B��ƽ��ʱ��n��C����0.48mol | |
| D�� | ��Ӧǰ2min��ƽ�����ʦͣ�C��=0.004mol•��L•min��-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������Ʊ�����ú���� | |
| B�� | Ũ�������ڹ���Լ�ƿ�� | |
| C�� | FeSO4��Һ����ڼ����������۵��Լ�ƿ�� | |
| D�� | ��ˮӦװ����ɫϸ��ƿ���ܷ�ܹⱣ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NO${\;}_{3}^{-}$��OH-��Cl- | B�� | Fe2+��OH-��NO${\;}_{3}^{-}$ | ||
| C�� | Fe2+��H+��Cl- | D�� | Na+��H+��OH- |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com