
在体积为1L的两个恒容密闭容器中,分别充入1molCO和1molH2O(g)的混合气体,进行如下化学反应:CO(g)+H2O(g)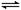 CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
|
|
0min |
10min |
20min |
30min |
40min |
50min |
|
830℃ |
1mol |
0.8mol |
0.65mol |
0.55mol |
0.5mol |
0.5mol |
|
1100℃ |
1mol |
0.75mol |
0.6mol |
0.6mol |
0.6mol |
0.6mol |
(1)1100℃时,前10min该反应的化学反应速率v(CO2)= ,830℃平衡后CO转化率的为__________________。
(2)1100℃时化学平衡常数K=_______,该反应为________反应(填“吸热”和“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是____________________。
(a)容器中压强不变 (b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O) (d)c(CO2)=c(CO)
(4)1100℃时达到平衡后,若向容器中再充入2molCO和2molH2O(g),平衡_____________________移动(选填“向正反应方向”或“向逆反应方向”或“不”),再达到平衡时,H2百分含量________________(选填“增大”或“减小”或“不变”)。
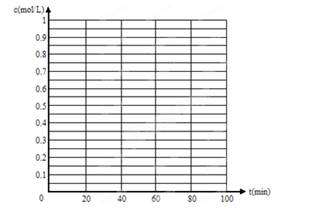
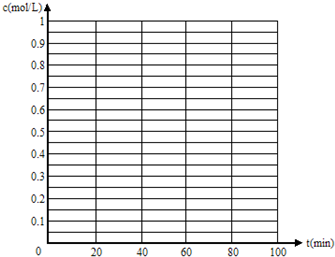
(5)830℃时,若在体积为2L的密闭容器中充入1molCO2和1molH2的混合气体,60min时反应达平衡状态,画出c(CO)和c(H2)随时间变化而变化的趋势图。
(1)0.025mol/(L·min) (1分) 50%(1分)
(2)4/9(或0.44)(2分) 放热(1分) (3)bc(2分)
(4)正反应方向 (1分) 不变(1分) (5)见图(两条曲线各2分,没标物质各扣0.5分)
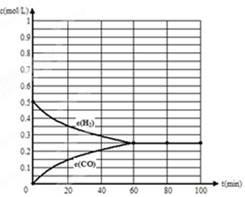
【解析】(1)1100℃时,前10min内CO的物质的量减少了0.25mol,所以生成CO2时0.25mol,则CO2的反应速率是0.25mol÷1L÷10min=0.025mol/(L·min) 。830℃平衡后剩余CO是0.5mol,所以,消耗CO是0.5mol,因此转化率是0.5÷1×100%=50%。
(2)1100℃平衡时CO(g)、H2O(g)、CO2(g)、H2(g)物质的量分别是0.6mol、0.6mol、0.4mol、0.4mol,所以平衡常数=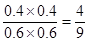 。温度越高平衡时CO的物质的量越大,说明升高温度平衡向逆反应方向移动,所以正反应是放热反应。
。温度越高平衡时CO的物质的量越大,说明升高温度平衡向逆反应方向移动,所以正反应是放热反应。
(3)在一定条件下,当可逆反应中正反应速率和逆反应速率相等时(但不为0),各种物质的浓度或含量均不再发生变化的状态,是化学平衡状态。所以b正确。平衡时浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系,d不正确。反应前后体积不变,所以压强始终是不变的,a不正确。C中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,正确,所以答案选bc。
(4)增大反应物的浓度,平衡向正反应方向移动。但由于反应前后体积不变的,且CO和水蒸气额物质的量之比还是1︰1的,所以平衡是等效的,因此氢气的含量不变。
(5)由于反应前后体积不变,在平衡是等效的,但平衡时各种物质的浓度均减半,所以图像为(见答案)。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
| 0min | 10min | 20min | 30min | 40min | 50min | |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省成都七中高二下学期期中考试化学试卷(带解析) 题型:填空题
在体积为1L的两个恒容密闭容器中,分别充入1molCO和1molH2O(g)的混合气体,进行如下化学反应:CO(g)+H2O(g)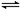 CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
CO2(g)+H2(g),反应物CO的物质的量在不同温度时物质的量随时间的变化如下表所示,回答下列问题:
| | 0min | 10min | 20min | 30min | 40min | 50min |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江西省高安中学高二上学期期末考试化学试卷(带解析) 题型:填空题
(共12分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
Ⅰ.目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3.25 mol H2,在一定条件下发生反应,测定CO2、CH3OH(g)和H2O(g)的浓度随时间变化如下图所示:
(1)从反应开始到平衡,氢气的平均反应速率 = mol/(L·min)
= mol/(L·min)
(2)该条件下CO2的转化率为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
| A.升高温度 | B.恒容时充入氮气 |
| C.将水蒸气从体系中分离 | D.用更有效的催化剂 |

查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省成都七中高二(下)期中化学试卷(解析版) 题型:解答题
| 0min | 10min | 20min | 30min | 40min | 50min | |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com