
| A、①>②>③>④>⑤ |
| B、②>③>⑤>④>① |
| C、③>①>②>⑤>④ |
| D、④>⑤>②>①>③ |
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
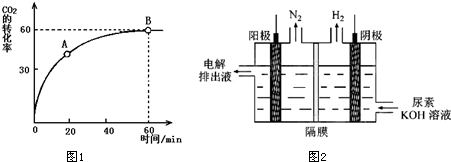
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molCl2作为氧化剂得到的电子数为NA |
| B、在标准状况下,11.2L水中含有分子数为0.5NA |
| C、0.3mol/LNa2SO4溶液中,所含Na+和SO42-总数为0.9NA |
| D、常温压下,64gSO2中含有的原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、锂(Li)的原子失电子能力比钠弱 |
| B、砹(At)的氢化物不稳定 |
| C、H2S比水稳定 |
| D、氢氧化钠比氢氧化镁的碱性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)2易被氧化生成Fe(OH)3,说明稳定性:Fe(OH)2<Fe(OH)3 |
| B、铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3(X=Cl、Br、I) |
| C、Fe与S加热可得FeS,所以Cu与S加热可得CuS |
| D、铁器放在潮湿的地方很容易生锈,其铁锈的主要成分Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、干冰和氨都属于弱电解质 |
| B、NO2和SO2都是形成酸雨的气体 |
| C、淀粉、纤维素和油脂都属于天然高分子化合物 |
| D、常温下,铁、铝遇到稀硝酸表面会生成一层致密的氧化膜,发生钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入少量CH3COONa固体 |
| B、通入少量氯化氢气体 |
| C、提高温度 |
| D、加入少量纯醋酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com