
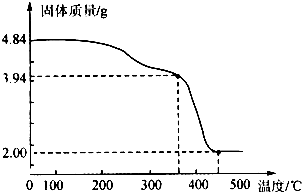
| 4.84g-3.94g |
| 18g/mol |
| 2.00g |
| 40g/mol |
|


科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、H2的燃烧热为-241.8kJ |
| B、2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol |
| C、1molH2完全燃烧生成液态水放出的热量大于241.8kJ |
| D、断开1molH2O的化学键吸收的总能量大于断裂1molH2和0.5 molO2的化学键所吸收的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 1 | 2 | 3 |
| 混合物质量/g | 4.36 | 5.54 | 9.81 |
| 硫酸溶液体积/mL | 50.00 | 50.00 | 50.00 |
| 生成SO2的物质的量/mol | 0.03 | 0.0375 | 0.03 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
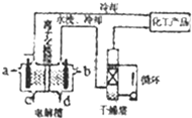 工业上电解饱和食盐水能制取多种化工原料,其设备示意图如图:
工业上电解饱和食盐水能制取多种化工原料,其设备示意图如图: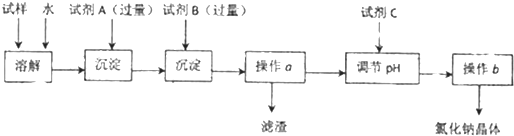
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
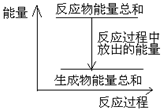 对于敞口容器中的反应:Zn(s)+H2SO4(aq)=ZnSO4 (aq)+H2(g),反应过程中能量关系可用右图表示,下列叙述中不正确的是( )
对于敞口容器中的反应:Zn(s)+H2SO4(aq)=ZnSO4 (aq)+H2(g),反应过程中能量关系可用右图表示,下列叙述中不正确的是( )| A、1 molZn的能量高于1 molH2的能量 |
| B、反应物Zn和H2SO4的总能量高于产物 ZnSO4和H2的总能量 |
| C、如果Zn足量,反应速率会经历由慢到快到慢的过程 |
| D、用锌粉代替锌粒,速率会加快 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com