
| A、该反应的离子方程式为:2I-+O3+H2O═2OH-+I2+O2 |
| B、反应中每1mol臭氧参加反应电子转移数为6mol |
| C、O2是该反应的还原产物 |
| D、由该反应可知氧化性的大小顺序:O3>O2 |


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
| A、升高温度,X的转化率增大 |
| B、缩小容器体积,Z的浓度不变 |
| C、保持压强不变,再充入0.1 mol X和0.1 mol Y,X的体积分数增大 |
| D、保持容器体积不变,充入一定量的氦气,Y的浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
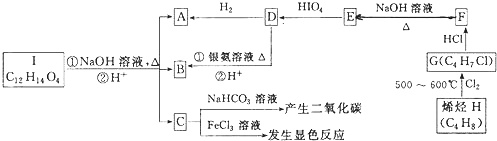
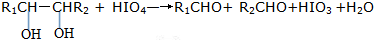
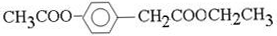
| 500~600℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胶体粒子直径在lnm~100nm |
| B、遇BaCl2溶液或Fe(OH)3胶体可发生聚沉 |
| C、电泳时,该胶体向阴极方向移动 |
| D、Na+使此胶体凝聚的效果不如Ca2+、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2中混有HCl(NaOH溶液) |
| B、FeCl3溶液中混有FeCl2(Cl2) |
| C、SiO2中混有Fe2O3(盐酸) |
| D、Fe2O3中混有SiO2(NaOH溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:
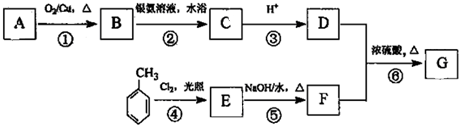
查看答案和解析>>
科目:高中化学 来源: 题型:
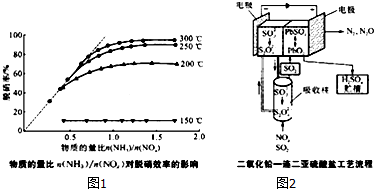
| 编号 | 名称 | 原理 |
| 方法一 | 尿素法 | 在温度70-95℃时,尿素溶液吸收NO、NO2,将其转化为N2 |
| 方法二 | 选择性催化还原( SCR)法 | 以NH3等作为还原剂,将烟气中的NOx还原生成N2和H2O |
| 方法三 | 电学法 | 以连二亚硫酸盐为氧化还原中介剂,将NOx还原为N2和N2O,连二亚硫酸盐被氧化成SO32-,经电化学还原而重复使用.采用内电池模式将SO2氧化为硫酸,在外电池模式时,电池可再生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com