
| 微粒 | ClO- | ClO2- | ClO3- | ClO4- |
| 立体结构 |




| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
 ,溴和碘都是非金属元素,二者之间易形成共价键,
,溴和碘都是非金属元素,二者之间易形成共价键, ;共价键;
;共价键; ,
, .
.

 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案科目:高中化学 来源: 题型:
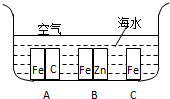 金属具有良好的导电、导热及延展性等,因此广泛应用于制造各种材料.请回答下列问题:
金属具有良好的导电、导热及延展性等,因此广泛应用于制造各种材料.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| O | - 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
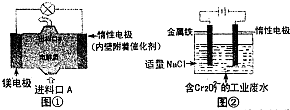 电化学在日常生活中用途广泛,图①是镁一次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图②是Cr2O2-7的工业废水的处理.下列说法正确的是( )
电化学在日常生活中用途广泛,图①是镁一次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图②是Cr2O2-7的工业废水的处理.下列说法正确的是( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com