


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:058
称取三份锌粉,分别盛于甲、乙、丙三支试管中,按下列要求另加物质后,塞上导管塞子,一定时间测定生成氢气的体积.甲加入50mLpH=3的盐酸,乙加入50mLpH=3的醋酸,丙加入50mLpH=3的醋酸和一定量的 粉末.若反应结束,生成
粉末.若反应结束,生成 的体积一样多,且没有锌粉剩余,请回答:
的体积一样多,且没有锌粉剩余,请回答:
(1)开始时反应速率大小顺序为__________.
(2)三支试管中参加反应的锌的质量大小顺序为_____________________.
(3)反应结束时,所需时间长短顺序为_____________________________.
(4)在反应过程中,乙、丙反应速率不同的理由是
__________________________
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
称取三份锌粉,分别盛于甲、乙、丙三支试管中,按下列要求另加物质后,塞上导管塞子,一定时间测定生成氢气的体积.甲加入50mLpH=3的盐酸,乙加入50mLpH=3的醋酸,丙加入50mLpH=3的醋酸和一定量的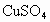 粉末.若反应结束,生成
粉末.若反应结束,生成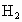 的体积一样多,且没有锌粉剩余,请回答:
的体积一样多,且没有锌粉剩余,请回答:
(1)开始时反应速率大小顺序为__________.
(2)三支试管中参加反应的锌的质量大小顺序为_____________________.
(3)反应结束时,所需时间长短顺序为_____________________________.
(4)在反应过程中,乙、丙反应速率不同的理由是
__________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com