
| A. | 氧化钙、熟石灰、CaO、碱性氧化物 | B. | 氢氯酸、盐酸、HCl、酸 | ||
| C. | 碳酸钠、纯碱、Na2CO3、碱 | D. | 硫酸铜、胆矾、CuSO4、盐 |
分析 A.根据常见物质的名称、俗名、化学式来判断,熟石灰为氢氧化钙;
B.氢氯酸是盐酸的化学名称,盐酸是俗名,其化学式为HCl;
C.碳酸钠为盐;
D.硫酸铜结晶水合物为胆矾.
解答 解:A.氧化钙成分为CaO,俗称为生石灰,和酸反应生成盐和水,属于碱性氧化物,熟石灰是氢氧化钙属于碱,名称、俗名、化学式及分类一不致,故A错误;
B.盐酸是氢氯酸的俗称,其化学式为HCl,故该组物质(或主要成分)的名称和化学式表示的是同一种物质,故B正确;
C.碳酸钠俗称为纯碱,化学式为Na2CO3、属于盐,名称、俗名、化学式及分类不都一致,故C错误;
D.硫酸铜结晶水合物俗称为胆矾,化学式为CuSO4•5H2O,属于盐,名称、俗名、化学式及分类不都一致,故D错误;
故选B.
点评 本题考查了物质组成、名称、俗称等,熟悉常见物质的化学式,和名称及俗名,是解此类题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 铝片与稀H2SO4反应 | B. | 灼热的炭与CO2反应 | ||
| C. | 高温煅烧石灰石 | D. | 甲烷在O2中的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
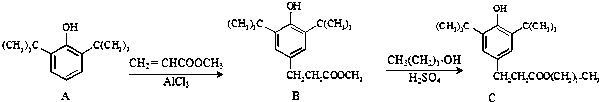
| A. | 物质A中所有碳原子有可能位于同一平面 | |
| B. | 物质B可与4molH2发生加成反应 | |
| C. | 用酸性KMnO4溶液鉴别抗氧化剂C中是否含有CH3(CH2)17OH | |
| D. | B生成C的反应类型为取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素 | 有关信息 |
| X | 元素主要化合价-2,原子半径为0.0074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 单质在X的单质中燃烧,产物是造成酸雨的罪魁祸首之一 |
| D | 最高价氧化物对应的水化物能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中的常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
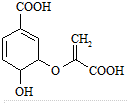
| A. | 分枝酸分子中含有2种官能团 | |
| B. | 分枝酸可与乙醇发生酯化反应 | |
| C. | 分枝酸是芳香族化合物 | |
| D. | 1mol分枝酸最多可与3molNaOH发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下0.1 mol/L的下列溶液①NH4Al(SO4)2、②NH4Cl、③NH3•H2O、④CH3COONH4溶液中,c(NH4+)由大到小的顺序是②>①>④>③ | |
| B. | 常温下0.4 mol/L CH3COOH溶液和0.2 mol/L NaOH溶液等体积混合后溶液显酸性,则溶液中粒子浓度大小顺序为:c(CH3COOH)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | 0.1 mol/L(NH4)2Fe(SO4)2溶液:c(NH4+)+c(NH3•H2O)+c(Fe2+)=0.3 mol/L | |
| D. | 室温下,向0.1 mol/LNH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
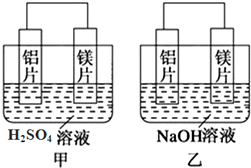
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com