
��ͼ��ijѧУʵ���Ҵ��г���ص��Լ���ǩ�ϵIJ������ݡ��ݴ�����˵����ȷ����

A��������Ͱ�ˮ�����ʵ���Ũ�ȷֱ�ԼΪ18��4mol��L��1��6��3mol��L��1
B����ȡ5mL���������ˮ��Ϻ�C��H2SO4��< 9��2mol��L��1,C��NH3��>6��45mol��L��1
C����ȡ5mL��������ˮ��Ϻأ�H2SO4��<49%,�أ�NH3��>12��5%
D����ȡ10mL�����ձ���,�ٷֱ����һ������ˮ���ɵõ���ϡ��������Һ�Ͱ�ˮ
 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ɹŰ������߶���10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪298Kʱ��Ӧ2SO2�� g ��+ O2�� g �� 2SO3�� g ������H = -197 kJ �� mol-1 ������ͬ�¶�����һ�ܱ������м���2 mol SO2��1 molO2 ���ﻯѧƽ��ʱ�ų�����Ϊa1 kJ ������һ�ݻ���ͬ���ܱ�������ͨ�� 1 mol SO2��0��5 molO2 ���ﻯѧƽ��ʱ�ų�����Ϊa2 kJ ,�����й�ϵʽ����ȷ����
2SO3�� g ������H = -197 kJ �� mol-1 ������ͬ�¶�����һ�ܱ������м���2 mol SO2��1 molO2 ���ﻯѧƽ��ʱ�ų�����Ϊa1 kJ ������һ�ݻ���ͬ���ܱ�������ͨ�� 1 mol SO2��0��5 molO2 ���ﻯѧƽ��ʱ�ų�����Ϊa2 kJ ,�����й�ϵʽ����ȷ����
A��a2 ��a1�� 197 B��2a2 ��a1 ��197
C��2a2 = a1 ��197 D��2a2 = a1 = 197
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ�ڵڶ��μ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�������ʹ�û������ȷ����
A���ձ�����ƿ����ƿ���ɼӵ�ʯ��������
B���Լ�ƿ�������ڴ�š��ܽ⡢ϡ��ҩƷ
C��������ƿ������Һʱ����������ˮ��Ҫ�ò����������������̶���
D���õζ�����ȡҺ��ʱ����ʼ�����������������ӣ�����ȡ�����ȷ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���Ϻ��и�����ѧ�����ײ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�л�������������ʣ��ܷ���������Ӧ������ʯ����Һ����ɫ������������Һ�������̪��Һ��������ɫ��ʧ��ԭ�л��������������е�
A������ B��������� C����ȩ D����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶������п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
Ϊ�˳��Ȼ�ͭ������Һ�е�Fe3+,���ڼ��������¼���һ���Լ�,���Լ���
A���������� B������ C������ͭ D����ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ��һ�ϵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��40%���ܶ�Ϊ1��43g/mL����NaOH��Һ������ˮ��ϣ�������Һ�����ʵ�����������
A������20% B��С��20% C������20% D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���Ĵ�������ѧ��һ��10�½β⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA���������ӵ���������ֵ������˵����ȷ����
A��1mol CO2�� SO3�Ļ��������ԭ����Ϊ 2NA
B��1mol/L KClO3 ��Һ�к��� NA��ClO3-
C����״���£� 11��2LCCl4�����ķ�����Ϊ 0��5 NA
D��25�棬1��01�� 105Pa��88gCO2������ԭ����Ϊ 6NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
��16�֣�ʵ���Ҳⶨ̼���� ��̼�����ƻ������̼���Ƶ���������W��Na2CO3������ȡ�˻����5��0g������ˮ�У����250 mL��Һ��
��̼�����ƻ������̼���Ƶ���������W��Na2CO3������ȡ�˻����5��0g������ˮ�У����250 mL��Һ��
����һ�������������û�ѧ��Ӧ��HCO3����CO32����ȫת��Ϊ��������������������������ɴ˼��������Цأ�Na2CO3����
��1����ȡ100 mL���ƺõ���Һ���ձ��У��μ�����������������Һ��HCO3����CO32����ȫת��Ϊ������Ӧѡ�õ��Լ��� �����ţ���
A��CaCl2��Һ B��MgSO4��Һ C��NaCl��Һ D��Ba��OH��2��Һ
��2�����ˣ�ϴ�ӳ������жϳ����Ƿ�ϴ���ķ����� ��
��3�������ó�����ָ����������������Ϊmg���ɴ˿��Լ���أ�Na2CO3��������˲��У�����δ�����־ͳ��������æأ�Na2CO3�� ���ƫ����ƫС"����Ӱ�족����
������������������ȡ10��00 mL���ƺõ���Һ������ϡ������Һ��Ӧ���ⶨ����������ͨ��״����Լ20�桢1��01��105 Pa����������ɴ˼��������Цأ�Na2CO3����
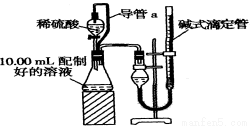
��1��װ���е���a��������  ��
��
��2������ȥ����a��ʹ���������� ����ƫ����ƫС������Ӱ�족����
���������ζ�������ȡ25��00 mL���ƺõ���Һ������ƿ�У��μ�2�η�̪�Լ���ҡ�ȣ���0��2000 mol/L������ζ����յ㣨��֪�յ�ʱ��ӦH++CO32��=HCO3��ǡ����ȫ�����ظ��˲���2�Σ�������������ƽ��ֵΪ20��00 mL��
��1����ȡ25��00 mL���ƺõ���Һ��Ӧѡ�� ��������ɡ�
��2���жϵζ��յ�������� ��
��3���˷���æأ�Na2CO3��= ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ����ʦ��Ʒ�Ƽ��������棩 ���ͣ�?????
1 mol����������2 mol̼������ �����Ϻ����ܱ������м��ȳ�ַ�Ӧ���ų��������ʺ���ȴ�������Ĺ���������
�����Ϻ����ܱ������м��ȳ�ַ�Ӧ���ų��������ʺ���ȴ�������Ĺ���������
A��Na2CO3 B��Na2O2 Na2CO3
C��NaOH Na2CO3 D��Na2O2 NaOH Na2CO3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com