
| A. | CO2和CH4都是引起“温室效应”的气体 | |
| B. | Na2O、Na2O2的组成元素相同,但阳离子和阴离子的数目比不同 | |
| C. | SO2、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 分别向新制氯水和久置氯水中滴加少量紫色石蕊试液,充分振荡后溶液都呈红色 |
分析 A.CO2和CH4都可导致全球温度升高;
B.Na2O、Na2O2的组成元素相同,阳离子均为钠离子,但阴离子分别为O2-、O22-;
C.NO易被空气中的氧气氧化;
D.新制氯水含HClO,而久置氯水不含HClO.
解答 解:A.CO2和CH4都可导致全球温度升高,则CO2和CH4都是引起“温室效应”的气体,故A正确;
B.Na2O、Na2O2的组成元素相同,阳离子均为钠离子,但阴离子分别为O2-、O22-,则阳离子和阴离子的数目比均为2:1,故B错误;
C.NO易被空气中的氧气氧化,SO2、NO、NO2都是大气污染气体,只有NO不能稳定存在,故C错误;
D.新制氯水含HClO,而久置氯水不含HClO,分别加紫色石蕊试液,充分振荡后,新制溶液呈无色,而久置氯水为红色,故D错误;
故选A.
点评 本题考查物质的性质及应用,为高频考点,把握物质的组成、性质、发生的反应为解答的关键,注意化学与环境的关系,题目难度不大.


 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
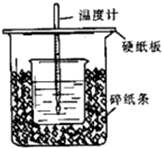 用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯分子中C原子均以sp3杂化方式成键,形成夹角为120°的三个sp3杂化轨道,故为正六边形的碳环 | |
| B. | 每个碳原子还有一个未参与杂化的2p轨道,垂直碳环平面,相互交盖,形成大π键 | |
| C. | 大π键中6个电子被6个C原子共用,故称为6中心6电子大π键 | |
| D. | 苯分子中共有十二个原子共面,六个碳碳键完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(H2)=0.2mol•L-1•min-1 | B. | v(N2)=0.2 mol•L-1•min-1 | ||
| C. | v(N2)=0.02 mol•L-1•s-1 | D. | v(H2)=0.04 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、苯都不能发生氧化反应 | |
| B. | 乙烯、聚乙烯都可与溴水发生加成反应 | |
| C. | 一氯丙烷(C3H7Cl)的同分异构体共有3种 | |
| D. | 乙酸乙酯、油脂与NaOH溶液反应均有醇类物质生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 000mL | B. | 500mL | C. | 100mL | D. | 1 500mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com