
【题目】试回答下列各问题:
(1)如图Ⅰ所示是1 mol NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________________________________________________________________________。
(2)化学反应的能量变化与反应物和生成物的键能有关。

①已知: H2(g)+Cl2(g) = 2HCl(g) ΔH=-185 kJ/mol;
E(H—H)=436 kJ/mol,E(Cl—Cl)=247 kJ/mol,则E(H—Cl)=________。
②图Ⅱ表示氧族元素中的氧、硫、硒、碲生成氢化物时的ΔH数据,根据ΔH数据可确定a、b、c、d分别代表哪种元素,试写出硒化氢在标准状况下,发生分解反应的热化学方程式:
________________________________________________________________________。
(3)已知:Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) ΔH=-25 kJ/mol ①
3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) ΔH=-47 kJ/mol ②
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) ΔH=+19 kJ/mol ③
请写出CO还原FeO的热化学方程式:_______________________________________________________。
【答案】(1)NO2(g)+CO(g) = NO(g)+CO2(g) ΔH=-234 kJ/mol
(2)①434 kJ/mol
②a代表Te b代表Se c代表S d代表O H2Se(g) = Se(s)+H2(g) ΔH=-81 kJ/mol
(3)FeO(s)+CO(g) = Fe(s)+CO2(g) ΔH=-11 kJ/mol
【解析】
试题分析:(1)根据图Ⅰ知1 mol NO2和CO反应生成CO2和NO放热234kJ,则NO2和CO反应的热化学方程式为NO2(g)+CO(g) = NO(g)+CO2(g) ΔH=-234 kJ/mol。
(2)①化学反应的焓变等于反应物的键能之和减去生成物的键能之和,则有DH=436 kJ/mol+247 kJ/mol-2 E(H—Cl)=-185 kJ/mol,则E(H—Cl)=434 kJ/mol ;②元素的非金属性越强,单质和氢气化合越越容易,生成的气态氢化物越稳定,放出的热量就越多,则a、b、c、d分别代表的元素是Te、Se、S、O;由图像知生成硒化氢的反应是吸热反应,则硒化氢为放热反应,热化学方程为H2Se(g) = Se(s)+H2(g) ΔH=-81 kJ/mol 。
(3)根据盖斯定律:①×3-②-③×2得6FeO(s) +6CO(g) ![]() 6Fe(s)+6CO2(g),则CO还原FeO的热化学方程式为FeO(s)+CO(g) = Fe(s)+CO2(g) ΔH=-11 kJ/mol。
6Fe(s)+6CO2(g),则CO还原FeO的热化学方程式为FeO(s)+CO(g) = Fe(s)+CO2(g) ΔH=-11 kJ/mol。


 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列关于物质分类的说法正确的是( )
A.稀豆浆、烟水晶、氯化铁溶液都属于胶体
B.Na2O、MgO、Mn2O7均属于碱性氧化物
C.氨水、冰醋酸、溴乙烷都属于弱电解质
D.葡萄糖、油脂、氨基酸都不属于有机高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.工业上可用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡 常数 | 温度/℃[ | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) | K3 | ||
(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=________(用K1、K2表示)。500 ℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol·L-1)分别为0.8、0.1、0.3、0.15,则此时v正________v逆(填“>”、“=”或“<”)。
(2)在3 L容积可变的密闭容器中发生反应②,已知c(CO)—反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是_______________。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是______________。

Ⅱ.利用CO和H2可以合成甲醇,反应原理为CO(g)+2H2(g) ![]() CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。
CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。 
(1)p1________p2(填“>”、“<”或“=”),理由是 。
(2)该甲醇合成反应在A点的平衡常数K= (用a和V表示)。
(3)该反应达到平衡时,反应物转化率的关系是CO________H2。(填“>”、“<”或“=”)
(4)下列措施中能够同时满足增大反应速率和提高CO转化率的是________(填字母)。
A.使用高效催化剂 B.降低反应温度
C.增大体系压强 D.不断将CH3OH从反应混合物中分离出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物由C、H、O三种元素组成,分子中含有8个原子,1mol该有机物含有46mol质子.完全燃烧该有机物在相同条件下测定CO2和水蒸气体积比为2:1。取2.7g该有机物恰好与30mL 1mol/L的碳酸钠溶液完全反应。(请写出必要的计算过程)求:
(1)有机物分子式;
(2)有机物结构简式.
(3)写出该有机物在一定条件下与乙二醇反应生成六元环状化合物的方程式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列17种物质或基团,根据要求填空。

(1)写出的电子式: 。
(2)按系统命名法命名 ,其发生消去反应可得到 几种烯烃。(要考虑立体异构)
(3)1 mol可与 mol⑧在光照条件下充分反应产生全氯代烷。
(4)写出⑨与新制的氢氧化铜悬浊液加热反应的化学反应方程式。
(5)上述物质中互为同系物的 ,互为同分异构体的 , (均填编号)
互为同位素的 ,互为同素异形体的 ,属于同种物质的 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了减少城市空气污染,要求使用无铅汽油,所谓无铅汽油是指( )
A.不用铅桶装的汽油
B.不含四乙基铅的汽油
C.不含Pb(NO3)2的汽油
D.不含氧化铅的汽油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 molX气体跟a molY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g)![]() b Z(g)。反应达到平衡后,测得X的转化率为25%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的5/6,则a和b的数值可能是( )
b Z(g)。反应达到平衡后,测得X的转化率为25%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的5/6,则a和b的数值可能是( )
A.a=2,b=1 B. a=1,b=2 C.a=2,b=2 D. a=3,b=2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学--选修5:有机化学基础]氰基丙烯酸酯在碱性条件下能快速聚合为![]() ,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
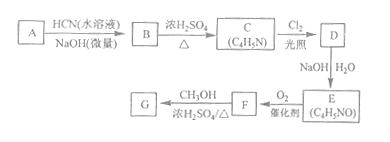
已知:①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A的化学名称为_______。
(2)B的结构简式为______,其核磁共振氢谱显示为______组峰,峰面积比为______。
(3)由C生成D的反应类型为________。
(4)由D生成E的化学方程式为___________。
(5)G中的官能团有___、 ____ 、_____。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有_____种。(不含立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一选修3:物质结构与性质】 碳是地球上组成生命的最基本元素之一,可以sp3 、sp2和sp杂化轨道成共价键,具有很强的结合能力,与其它元素结合成不计其数的无机物和有机化合物,构成了丰富多彩的世界。碳及其化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)基态碳原子核外有 种空间运动状态的电子,其价电子排布图为 。
(2)光气的分子式为COCl2,又称碳酰氯,是一种重要的含碳化合物,判断其分子立体构型为 ,其碳原子杂化轨道类型为 杂化。
(3)碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,如下表所示:
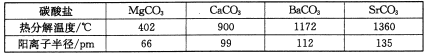
试解释为什么随着阳离子半径的增大,碳酸盐的分解温度逐步升高?
(4)碳的一种同素异形体——C60,又名足球烯,是一种高度对称的球碳分子。立方烷(分子式:C8H8,结构是立方体:![]() )是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
)是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
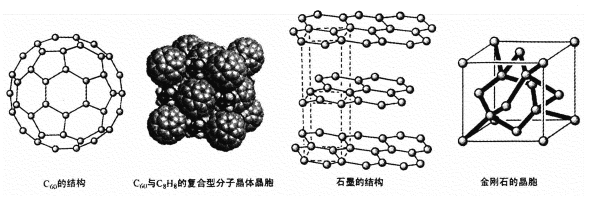
(5)碳的另一种同素异形体——石墨,其晶体结构如上图所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为 个。已知石墨的密度为ρg.cm-3 ,C-C键长为rcm,阿伏伽德罗常数的值为NA,计算石墨晶体的层间距为 cm。
(6)碳的第三种同素异形体—一金刚石,其晶胞如上图所示。已知金属钠的晶胞(体心立方堆积)沿其体对角线垂直在纸平面上的投影图如下图A所示,则金刚石晶胞沿其体对角线垂直在纸平面上的投影图应该是下图 (从A~D图中选填)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com