
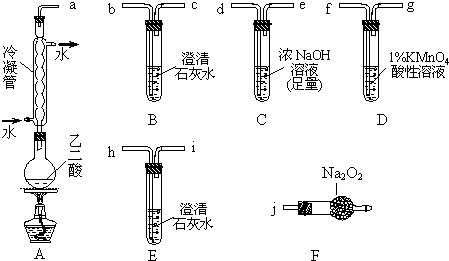
 两个学习小组用图装置探究乙二酸(HOOC-COOH)受热分解的部分产物.
两个学习小组用图装置探究乙二酸(HOOC-COOH)受热分解的部分产物. CO2↑+CO↑+H2O,故答案为:HOOC-COOH
CO2↑+CO↑+H2O,故答案为:HOOC-COOH CO2↑+CO↑+H2O;
CO2↑+CO↑+H2O; CO2↑+CO↑+H2O,检验产物时先通过澄清石灰水观察是否变浑浊,并通入到NaOH溶液除去CO2,然后通入酸性高锰酸钾溶液观察溶液颜色变化以判断是否有CO生成;
CO2↑+CO↑+H2O,检验产物时先通过澄清石灰水观察是否变浑浊,并通入到NaOH溶液除去CO2,然后通入酸性高锰酸钾溶液观察溶液颜色变化以判断是否有CO生成;

 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
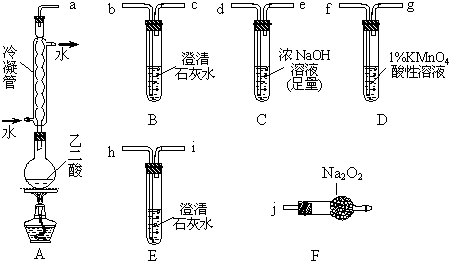
 (2009?重庆)两个学习小组用图装置探究乙二酸(HOOC-COOH)受热分解的部分产物.
(2009?重庆)两个学习小组用图装置探究乙二酸(HOOC-COOH)受热分解的部分产物.| 加热 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源:重庆 题型:问答题
查看答案和解析>>
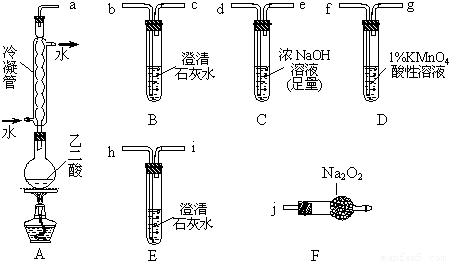
科目:高中化学 来源:2009-2010学年湖北省黄冈中学高三(上)月考化学试卷(8月份)(解析版) 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2009年重庆市高考化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com