
| A、某酸H2A的钠盐NaHA溶液中:c(A2-)<c(H2A),则该溶液的pH>7 |
| B、1.0×10-3 mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0 |
| C、在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
| D、Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 |


科目:高中化学 来源: 题型:
| c(OH-) |
| c(NH3?H2O) |
| A、①②③ | B、①③⑤ |
| C、①③⑥ | D、②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新制氯水可使无色酚酞试纸先变红,后褪色 |
| B、新制的氯水只含Cl2和H2O分子 |
| C、氯水放置数天后,酸性增强 |
| D、光照氯水有气泡逸出,该气体是Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
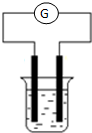 现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下:
现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下:| G 实验分组 | 所用金属 | 电子流向 |
| ① | A、Cu | A→Cu |
| ② | C、D | D→C |
| ③ | A、C | C→A |
| ④ | B、Cu | Cu→B |
| ⑤ | … | … |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+、O2、H2O2三种微粒都具有氧化性,没有还原性 |
| B、木炭与浓硝酸反应可能生成CO和NH4NO3 |
| C、因为SO2具有还原性,所以不能用浓H2SO4干燥SO2 |
| D、Cl2转变为HClO时一定需要加入氧化剂才能实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| T/K | T1 | T2 | T3 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、O原子的电子排布图为 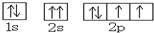 |
| B、氯化钠的分子式:NaCl |
C、Cl-的结构示意图: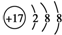 |
| D、Ca原子的电子排布式为 1s22s22p63s23p63d2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用盐酸清除水垢CaCO3+2H+=Ca2++CO2↑+H2O |
| B、Fe跟稀硫酸反应:Fe+2H+=Fe2++H2↑ |
| C、澄清石灰水跟稀盐酸:H++OH-=H2O |
| D、碳酸氢钠溶液跟氢氧化钠溶液反应 HCO3-+OH-=H2O+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com