
 4Na+2H2O+O2↑。后来盖·吕萨克用铁与熔融 氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是
4Na+2H2O+O2↑。后来盖·吕萨克用铁与熔融 氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是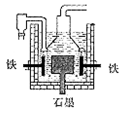
| A.电解熔融氢氧化钠制钠,阴极发生电极反应为:Na++e-=Na |
| B.盖·吕萨克法制钠原理是嫡的增加带动了反应的进行 |
| C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数比为1:1 |
| D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
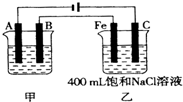
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
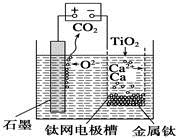
| A.由TiO2制得1 mol金属Ti,理论上外电路转移2 mol电子 |
| B.阳极的电极反应式为C+2O2--4e-=CO2↑ |
| C.在制备金属钛前后,整套装置中CaO的总量减少 |
| D.若用铅蓄电池作该装置的供电电源,“+”接线柱应连接Pb电极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
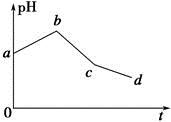
| A.整个过程中两电极反应2Cl--2e-=Cl2↑、2H++2e-=H2↑不可能同时发生 |
| B.电解至c点时,往电解液中加入适量CuCl2固体,即可使电解液恢复至原来的浓度 |
| C.ab段表示电解过程中H+被还原,pH上升 |
| D.原混合溶液中KCl和CuSO4的浓度之比恰好为2∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
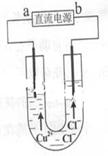
| A.a端是直流电源的负极 |
| B.通电使CuCl2发生电离 |
| C.阳极上发生的反应:Cu2++2e-=Cu |
| D.通电一段时间后,在阴极附近观察到黄绿色气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.都用粗铜作阳极、纯铜作阴极 |
| B.电解液的成分都保持不变 |
C.阳极反应都只有Cu-2e- Cu2+ Cu2+ |
D.阴极反应都只有Cu2++2e- Cu Cu |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.②③⑤ |
| C.③④ | D.①③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | S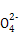 、OH- 、OH- |
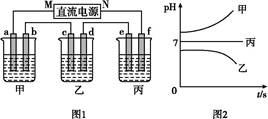
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com