
| A、自来水 |
| B、0.5mol?L-1盐酸 |
| C、0.25mol?L-1H2SO4 |
| D、0.5mol?L-1NH4NO3 |


科目:高中化学 来源: 题型:

| A、红褐色液体为氢氧化铁胶体 |
| B、加入石灰石是为了促进氯化铁水解 |
| C、产生的气泡是HCl气体 |
| D、产生的气泡是CO2 气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
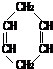 可简写为
可简写为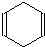 .现有某化合物W的分子结构可表示为:
.现有某化合物W的分子结构可表示为: .
.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将一小块Na投入水中,钠浮于水面,说明钠密度比水小 |
| B、将一小块Na投入滴有酚酞的水中,溶液变红,说明反应生成了碱 |
| C、将一小块Na投入CuSO4溶液中,生成蓝色沉淀,说明Na没有Cu活泼 |
| D、点燃Na与肥皂水反应产生的气泡,有尖锐爆鸣声,说明有H2生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3、FeCl2均可由化合反应制得 |
| B、配制1L0.1mol/LNa2CO3溶液,需称取Na2CO3?H2O的质量为10.6g |
| C、用澄清石灰水可鉴别CO2和SO2 |
| D、用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热NH4C1晶体时,将湿润的红色石蕊试纸靠近试管口,检验NH3的生成 |
| B、向某溶液中加入足量盐酸酸化,无现象,再加入BaCl2溶液,有白色沉淀生成,说明原溶液中存在SO42- |
| C、取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ |
| D、用饱和碳酸钠溶液除去二氧化碳中的氯化氢 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com