
 NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:
NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:| 时间(s) | 0 | 1 | 2 | 3 | 4 | … |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.00×10-4 | 1.70×10-4 | 1.00×10-4 | 1.00×10-4 | … |
分析 Ⅰ.(1)根据表格中数据算出前2s内的平均反应速率υ(NO)=(1.00×10-3-1.70×10-4 )÷2=4.15×10-4mol/(L•s),根据化学反应速率之比等于化学计量数之比,υ(N2)=1/2υ(NO)=2.08×10-4 mol/(L•s);由表格数据看出第3s后c(NO)不变则达平衡,此时c(CO)=1.00×10-4mol•L-1,c(CO2)=1.00×10-3mol•L-1 -1.00×10-4mol•L-1=9.00×10-4mol•L-1,c(N2)=1/2c(CO2)=4.50×10-4mol•L-1,根据K=c(CO2)2×c(N2)/(c(NO)2×c(CO)2)=3.65×106;
(2)达到平衡时,要提高NO转化率,即改变条件要使平衡正向移动,
A.选用更有效的催化剂,平衡不移动;
B.降低反应体系的温度,该反应为放热反应,正向移动;
C.充入氩气使容器内压强增大,平衡不移动;
D.充入CO使容器内压强增大,相当于增大CO浓度,平衡正向移动,NO转化率提高;
(3)由已知方程①2NO(g)+2CO(g)=2CO2(g)+N2(g)△H=-748kJ/mol及②N2(g)+O2(g)=2NO(g)△H=+180kJ/mol.根据盖斯定律①÷2+②÷2得CO的燃烧热的热化学方程式为CO(g)+1/2O2(g)=CO2(g)△H=(-748kJ/mol)÷2+(+180kJ/mol)÷2=-284 kJ/mol;
Ⅱ.(4)O3氧化NO结合水洗可产生HNO3和O2,转移电子数=化合价升高数,NO转化为HNO3 ,化合价升高3,每生成1mol的HNO3转移3mol电子;
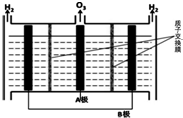
(5)根据已知图,A极出来的是O3,B极出来的是H2,说明A极发生的氧化反应为阳极,B极发生还原反应为阴极,阳极(惰性电极)的电极反应式为3H2O-6e-=O3+6H+
解答 解:Ⅰ.(1)根据表格中数据算出前2s内的平均反应速率υ(NO)=(1.00×10-3-1.70×10-4 )÷2=4.15×10-4mol/(L•s),根据化学反应速率之比等于化学计量数之比,υ(N2)=1/2υ(NO)=2.08×10-4 mol/(L•s);由表格数据看出第3s后c(NO)不变则达平衡,此时c(CO)=1.00×10-4mol•L-1,c(CO2)=1.00×10-3mol•L-1 -1.00×10-4mol•L-1=9.00×10-4mol•L-1,c(N2)=1/2c(CO2)=4.50×10-4mol•L-1,根据K=c(CO2)2×c(N2)/(c(NO)2×c(CO)2)=3.65×106,
故答案为:2.08×10-4 mol/(L•s);3.65×106;
(2)达到平衡时,要提高NO转化率,即改变条件要使平衡正向移动,
A.选用更有效的催化剂,平衡不移动,故A错误;
B.降低反应体系的温度,该反应为放热反应,正向移动,故B正确;
C.充入氩气使容器内压强增大,平衡不移动,故C错误;
D.充入CO使容器内压强增大,相当于增大CO浓度,平衡正向移动,NO转化率提高,故D正确.
故答案为:BD;
(3)由已知方程①2NO(g)+2CO(g)=2CO2(g)+N2(g)△H=-748kJ/mol及②N2(g)+O2(g)=2NO(g)△H=+180kJ/mol.根据盖斯定律①÷2+②÷2得CO的燃烧热的热化学方程式为CO(g)+1/2O2(g)=CO2(g)△H=(-748kJ/mol)÷2+(+180kJ/mol)÷2=-284 kJ/mol,
故答案为:284 kJ/mol;
Ⅱ.(4)O3氧化NO结合水洗可产生HNO3和O2,转移电子数=化合价升高数,NO转化为HNO3 ,化合价升高3,每生成1mol的HNO3转移3mol电子,故答案为:3;
(5)根据已知图,A极出来的是O3,B极出来的是H2,说明A极发生的氧化反应为阳极,B极发生还原反应为阴极,阳极(惰性电极)的电极反应式为3H2O-6e-=O3+6H+,
故答案为:B;3H2O-6e-=O3+6H+.
点评 本题考查了反应速率、平衡常数、转化率的计算,反应能量变化的分析判断和热化学方程式的书写,化学平衡的影响因素分析应用,平衡常数计算,电极方程式的书写等,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Na+的电子式: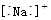 | B. | Na+的结构示意图: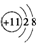 | ||
| C. | Na的电子排布式:1s22s22p63s1 | D. | Na的简化电子排布式:3s1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | [Cr(H2O)6]Cl3 | B. | [Cr(H2O)5Cl]Cl2•H2O | ||
| C. | [Cr(H2O)4Cl2]Cl•2H2O | D. | [Cr(H2O)3Cl3]•3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学反应 | 反应热 | 平衡常数(850℃) |
| ①CO (g)+2H2 (g)═CH3 OH(g) | △H1=-90.8kj/mol | k1=160(mol/L)-2 |
| ②CO2 (g)+H2 (g)═CO (g)+H2 O(g) | △H2=-41.2kj/mol | K2 |
| ③3H2 (g)+CO2 (g)═H2 O(g)+CH3 OH(g)△H 3 | △H3 | K3=160(mol/L)-2 |
| 物质 | H2 | CO2 | CH3OH | H2O |
| 浓度(mol/L) | 0.2 | 0.2 | 0.4 | 0.4 |
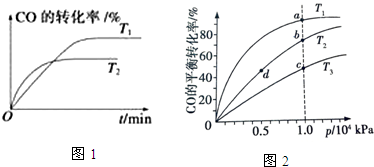
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
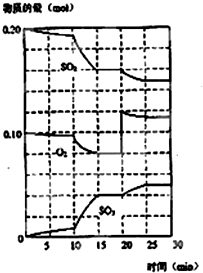 在一定条件下,二氧化硫和氧气发生如图反应:
在一定条件下,二氧化硫和氧气发生如图反应:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
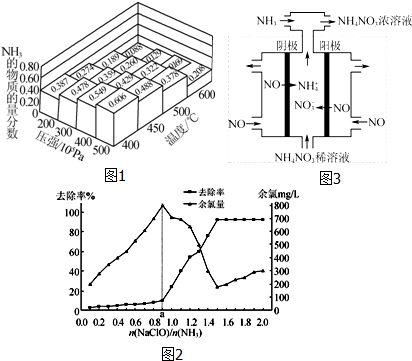
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
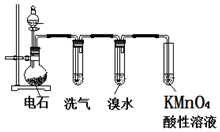 如图为实验室制取乙炔并验证其性质的装置图,回答下列问题:
如图为实验室制取乙炔并验证其性质的装置图,回答下列问题: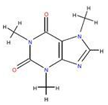 ,实验室可通过下列简单方法从茶叶中提取咖啡因:
,实验室可通过下列简单方法从茶叶中提取咖啡因: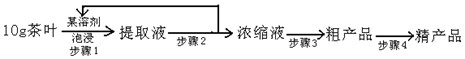
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com