
| A. | 开发太阳能、水能、风能、地热等新能源 | |
| B. | 减少资源消耗,注重资源的重复使用、资源的循环再生 | |
| C. | 大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 | |
| D. | 大力开采煤、石油和天然气,以满足人们日益增长的能源需求 |
分析 A、太阳能、水能、风能、地热等新能源无污染;
B、资源的再利用是对资源的一种节约;
C、沼气是可再生能源;
D、化石燃料是不可再生的.
解答 解:A、太阳能、水能、风能、地热等新能源无污染,且太阳能、风能取之不尽用之不竭,这些能源的开发能大大解决人类能源紧缺的问题,故A正确;
B、资源的再利用是对资源的一种节约,且能减少污染,故利于开源节流,故B正确;
C、沼气是可再生能源,且能对废弃的秸秆再利用,故属于开源节流,故C正确;
D、化石燃料是不可再生的,故大力开采煤、石油和天然气不属于开源节流,故D错误.
故选D.
点评 本题考查了能源的利用,注意可再生能源和不可再生能源的利用,难度不大.


科目:高中化学 来源: 题型:解答题
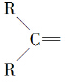 ”生成酮,“
”生成酮,“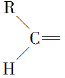 ”生成“
”生成“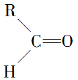 ”,
”,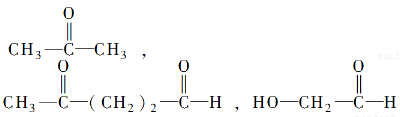
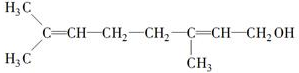 或
或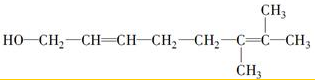 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | SO2的催化氧化反应是吸热反应 | |
| B. | SO2的转化率一定为20% | |
| C. | 导出气体中SO3所占的体积分数为$\frac{2}{9}$ | |
| D. | 单位时间内进人接触室的气体与从接触室导出的气体的物质的量之比为10:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质内部储存的能量--化学反应的热效应 | |
| B. | 分子间作用力的大小--分子稳定性的高低 | |
| C. | 原子核外电子排布--元素在周期表中的位置 | |
| D. | 有效碰撞几率的高低--化学反应速率的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
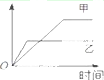 表格中的各种情况,可以用如图的曲线表示的是( )
表格中的各种情况,可以用如图的曲线表示的是( ) | 反 应 | 纵坐标 | 甲 | 乙 | |
| A | 相同质量的氨,在同一容器中 2NH3═N2+3H2 △H<0 | 氨气的转化率 | 500℃ | 400℃ |
| B | 等质量钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
| C | 向温度和压强都相同的甲乙两容器中分别投入体积比1:3的N2、H2(N2+3H2═2NH3) | 氨气的物质的量 | 反应过程中保持恒温恒容 | 反 应过程中保持恒温恒压 |
| D | 2molSO2和1molO2,在相同温度下 2SO2+O2═2SO3 | SO3 的浓度 | 2个大气压 | 10个大气压 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
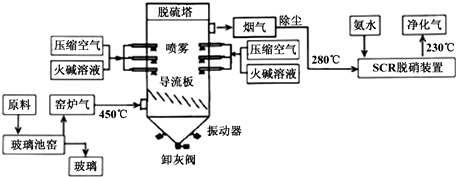
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为减少环境污染,常使用乙醇汽油代替化石燃料,乙醇可通过纤维素转化制得,是一种可再生的燃料 | |
| B. | 优良的催化剂可以降低反应温度,起到节能效果并提高反应物的转化率 | |
| C. | 分光光度计可用于分析溶液颜色与反应物(或生成物)浓度的关系,从而确定化学反应速率 | |
| D. | 某些铝硅酸盐形成的分子筛中有许多笼状空穴和通道,常用于分离、提纯气体或液体混合物,还可作干燥剂、催化剂载体等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com