
【题目】艾司洛尔是预防和治疗手术期心动过速或高血压的一种药物,艾司洛尔的一种合成路线如下:

回答下列问题:
(1)丙二酸的结构简式为_______;E中含氧官能团的名称是_______。
(2)D生成E的反应类型为____________。
(3)C的结构简式为________________。
(4)A遇FeCl3溶液发生显色反应,1 mol A和1 mol丙二酸在吡啶、苯胺中反应生成1 mol B、1 mol H2O和1 mol CO2,B能与溴水发生加成反应,推测A生成B的化学方程式为____。
(5)X是B的同分异构体,X同时满足下列条件的结构共有____种,其中核磁共振氢谱有五组峰的结构简式为____。
①可与碳酸氢钠溶液反应生成二氧化碳
②遇FeCl3溶液发生显色反应
③除苯环外不含其他环
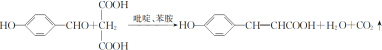
(6)写出以苯甲醇和丙二酸为原料制备![]() 的合成路线________(其他试剂任选)。
的合成路线________(其他试剂任选)。
【答案】HOOC-CH2-COOH 醚键、酯基 取代反应 ![]()
 15
15 ![]()
【解析】
本题主要考查有机合成综合推断以及逆向合成。合成路线由E的结构简式以及D的分子式可推断出D的结构简式为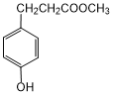 ,由C与甲醇发生酯化反应生成D,可推断出C的结构简式为
,由C与甲醇发生酯化反应生成D,可推断出C的结构简式为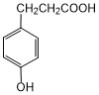 ,B与氢气发生加成反应生成C,结合B的分子式与第(4)问中“B能与溴水发生加成反应”,可推断出B的结构简式为
,B与氢气发生加成反应生成C,结合B的分子式与第(4)问中“B能与溴水发生加成反应”,可推断出B的结构简式为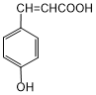 ,A与丙二酸在吡啶、苯胺中反应生成B,结合A的分子式以及第(4)问中“A遇FeCl3溶液发生显色反应,1 mol A和1 mol丙二酸在吡啶、苯胺中反应生成1 mol B、1 mol H2O和1 mol CO2”,可推断出A的结构简式为
,A与丙二酸在吡啶、苯胺中反应生成B,结合A的分子式以及第(4)问中“A遇FeCl3溶液发生显色反应,1 mol A和1 mol丙二酸在吡啶、苯胺中反应生成1 mol B、1 mol H2O和1 mol CO2”,可推断出A的结构简式为![]() 。
。
(1)丙二酸的结构简式为:![]() ;观察E结构简式可知,所含含氧官能团有:醚键、酯基;
;观察E结构简式可知,所含含氧官能团有:醚键、酯基;
(2)D生成E的方程式为: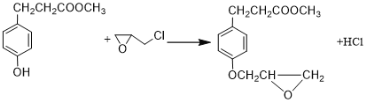 ,故反应类型为取代反应;
,故反应类型为取代反应;
(3)由上述分析可知,C的结构简式为: ;
;
(4)根据化学方程式配平可写出A生成B的化学方程式为: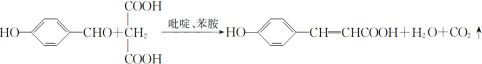 ;
;
(5)条件①:该结构简式中含有羧基;条件②:该结构简式中含有酚羟基;条件③:除苯环外,不含有其它杂环;可以酚羟基作为移动官能团,书写出主要碳骨架,再进行判断同分异构体总数,(1)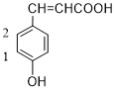 中酚羟基有2个取代位置(不包含本身),(2)
中酚羟基有2个取代位置(不包含本身),(2)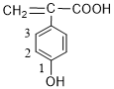 中酚羟基有3个取代位置,(3)
中酚羟基有3个取代位置,(3)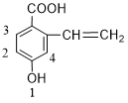 中酚羟基有4个取代位置,(4)
中酚羟基有4个取代位置,(4)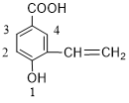 中酚羟基有4个取代位置,(5)
中酚羟基有4个取代位置,(5)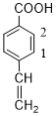 中酚羟基有2个取代位置,故同分异构体一共有2+3+4+4+2=15种;核磁共振氢谱有五组峰的结构简式为
中酚羟基有2个取代位置,故同分异构体一共有2+3+4+4+2=15种;核磁共振氢谱有五组峰的结构简式为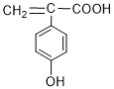 。
。
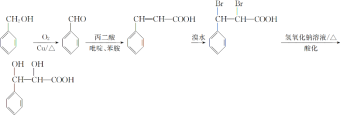
(6)对比苯甲醇和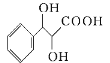 结构简式,根据题干信息,需将苯甲醇氧化生成苯甲醛,再模仿A生成B的方程式生成
结构简式,根据题干信息,需将苯甲醇氧化生成苯甲醛,再模仿A生成B的方程式生成 ,再根据碳碳双键与卤素单质加成再取代合成
,再根据碳碳双键与卤素单质加成再取代合成 ,故合成路线为:
,故合成路线为:


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】对可逆反应2A(s)+3B(g)![]() C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
①增加A的量,平衡向正反应方向移动
②升高温度,反应速率增大,平衡向逆反应方向移动
③压缩容器增大压强,平衡不移动,v正、v逆不变
④增大B的浓度,v正>v逆
⑤加入催化剂,B的转化率提高
A.①②B.②④C.①③D.②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一块擦去氧化膜的铝片放入20 mL 0.5 mol·L-1 CuSO4溶液中,观察实验现象。下列方程式不正确的是
A.Cu2+(aq)+2H2O(l)Cu(OH)2(s)+2H+(aq) △H>0
B.2Al(s)+3Cu2+(aq)=2Al3+(aq)+3Cu(s) △H<0
C.Cu(OH)2(s)![]() CuO(s)+H2O(l) △H>0
CuO(s)+H2O(l) △H>0
D.2Al(s)+6H+(aq)=2Al3+(aq)+3H2(g) △H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)比较金属性的强弱:Na_________K(填“>”、“<”或“=”);反应Na+KClNaCl+K↑能发生的原因是________________。
(2)COCl2是共价化合物,各原子均满足8电子稳定结构。写出COCl2的结构式__________。
(3)电解熔融氧化铝制备金属铝时,需要定期更换阳极石墨块,理由是_________________(用化学反应方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸是一种二元弱酸,可用作还原剂、沉淀剂等。某校课外小组的同学设计利用C2H2气体制取H2C2O4·2H2O。回答下列问题:
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。

①电石与水反应很快,为了减缓反应速率,装置A中除用饱和食盐水代替水之外,还可以采取的措施是__________(写一种即可)。
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为______。该过程中,可能产生新的杂质气体Cl2,其原因是: _____________(用离子方程式回答)。
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是______________________。
②装置D中生成H2C2O4的化学方程式为____________________________。
③从装置D中得到产品,还需经过_____________(填操作名称)、过滤、洗涤及干燥。
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是______________________。
②滴定过程中发现褪色速率开始很慢后逐渐加快,分析可能的原因是_______________。
③产品中H2C2O4·2H2O的质量分数为_______________(列出含 m、c、V 的表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳在冶金工业上具有重要用途。已知氧与碳的反应主要有:
Ⅰ.C(s)+O2(g)CO2(g) △H1=-394kJ·mol-1
Ⅱ.2C(s)+O2(g)2CO(g) △H2=-221kJ·mol-1
Ⅲ.2CO(g)+O2(g)2CO2(g) △H3
上述反应的△G~T如图所示,且满足△G=△H-T△S。
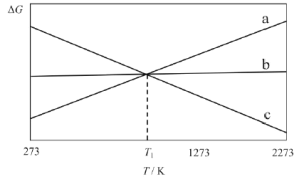
请回答:
(1)曲线a代表反应_________(填“I”、“II”或“III”),理由是__________。
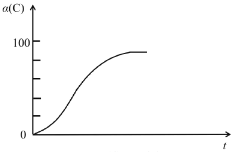
(2)研究发现,以CO2替代高温水蒸气作为煤气化反应(H2O与C反应)的气化剂,实现了CO2零排放的新工艺。写出反应IV的热化学方程式___________(碳的计量数为1)。在1273K时,测得碳转化率[α(C)]与时间t变化如图所示。保持其它条件不变,请画出1773K时α(C)~t关系图______。
(3)当T=T1时,反应IV处于平衡状态,下列关于反应IV的说法正确的是_________。
A.因平衡时△G=0,若△H变化173.3kJ·mol-1,△S变化173.3J·K-1·mol-1,计算得T1=1000K
B.T<T1时,反应向逆反应方向移动
C.当碳的浓度不再变化时,一定处于平衡状态
D.因平衡常数K的值不再变化,反应达到了平衡
(4)当T=1273K时,仅存在CO、CO2两种气体,且维持总压为1 atm,此时反应IV的Kp=112,则CO气体所占的分压p(CO)为___________atm。(列式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,用浓度为0.1000 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.1000 mol·L-1的三种酸HX、HY、HZ,滴定曲线如下图所示。下列说法错误的是
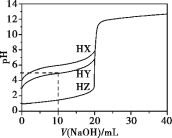
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HX<HY<HZ
B.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+)
C.根据滴定曲线,可得知Y-的水解常数K约为10-9
D.由图象可知酸碱中和滴定分析不适用于极弱的酸和极弱的碱的测定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于如下反应,其反应过程的能量变化示意图如图:
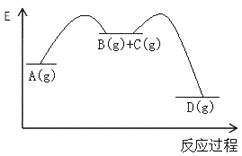
编号 | 反应 | 平衡常数 | 反应热 |
反应① | A(g)=B(g)+C(g) | K1 | △H1 |
反应② | B(g)+C(g)=D(g) | K2 | △H2 |
反应③ | A(g)= D(g) | K3 | △H3 |
下列说法正确的是
A.K3 =K1 + K2B.△H3=△H1+△H2
C.加催化剂,反应①的反应热降低,反应速率加快D.则增大压强,K1减小,K2增大,K3不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如下物质的转化关系图,回答有关问题:

(1)上述物质中,_________(填结构简式,下同)的产量是衡量一个国家石油化工发展水平的标志;常见的酸性调味品中含有3%~5%的_________;具有香味的油状液体是_____________。
(2)乙烯的工业制法是_________。
a.石油裂化 b.煤干馏 c.石油裂解 d.石油分馏
(3)乙醛中的官能团名称是______,比乙醛少一个碳原子的同系物的结构简式是______。
(4)工业上用乙烯水化法制乙醇,乙烯在加热、加压和催化剂存在的条件下,跟水反应生成乙醇,该反应的化学方程式是_______________________。
(5)生成乙酸乙酯的化学方程式是__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com