
| A、等于p% | B、大于p% |
| C、小于p% | D、无法判断 |


科目:高中化学 来源: 题型:
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp(25℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| A、向混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀 |
| B、向溶液中加入双氧水,并用CuO粉末调节pH,过滤后可获得溶质主要为CuSO4的溶液 |
| C、该溶液中c(SO42-):[c(Fe3+)+c(Fe2+)+c(Cu2+)]=5:4 |
| D、将少量FeCl3粉末加入含Cu(OH)2的悬浊液中,其中c(Cu2+)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 浓溴水 | 过滤 |
| B | 溴苯(Br2) | 苯 | 分液 |
| C | 乙醇(水) | Na | 蒸馏 |
| D | 甲烷(乙烯) | 溴水 | 洗气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 -X、
-X、 -Y,
-Y, -Z.其对应的化学式不正确的是( )
-Z.其对应的化学式不正确的是( )A、 XY |
B、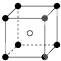 X2Y |
C、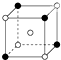 X3Y |
D、 XY3Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、①② |
| C、① | D、①②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下,向O.1mol?L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的质量与加入氢氧化钡溶液的体积关系如图所示,下列有关说法中正确的是( )
常温下,向O.1mol?L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的质量与加入氢氧化钡溶液的体积关系如图所示,下列有关说法中正确的是( )| A、溶液的导电能力:a>b>c>d |
| B、溶液的pH:a<b<c<d |
| C、b溶液中的H+浓度和d溶液中的OH-浓度相等 |
| D、c溶液和d溶液都呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体的压强 |
| B、混合气体的密度 |
| C、B的物质的量浓度 |
| D、气体的平均相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 S2Cl2广泛用于橡胶工业,其分子结构如图所示.常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体.下列说法不正确的是( )
S2Cl2广泛用于橡胶工业,其分子结构如图所示.常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体.下列说法不正确的是( )| A、S2Cl2与H2O反应的化学方程式为2S2Cl2+2H2O═SO2↑+3S↓+4HCl |
| B、S2Cl2分子中含有极性键和非极性键 |
| C、S2Br2与S2Cl2结构相似,熔、沸点:S2Br2>S2Cl2 |
| D、S2Cl2中S-S键键能大于S-Cl键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、核外电子总是优先排在能量最低的电子层上 |
| B、K层是能量最低的电子层 |
| C、N电子层为次外层时,最多可容纳的电子数为18 |
| D、各电子层(n)最多可容纳的电子数为n2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com