
【题目】下列离子方程式正确的是( )
A. 过氧化钠加入水中:2O22-+2H2O== 4OH-+O2↑
B. 碳酸氢钠溶液加入盐酸:CO32-+2H+==CO2↑+H2O
C. 氢氧化铜中加入盐酸:OH-+H+==H2O
D. 四氧化三铁跟稀硫酸反应:Fe3O4+8H+==Fe2++2Fe3+ +4H2O
科目:高中化学 来源: 题型:
【题目】用质量分数98%、密度为1.84gcm﹣3的浓硫酸配制480mL0.92molL﹣1的稀硫酸
(1)配制时,除量筒、烧杯、玻璃棒外还需玻璃仪器有、 .
(2)减小误差量取时需选用合适的量筒量取mL浓硫酸
(3)在容量瓶的使用方法中,下列操作不正确的是 .
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2cm处,改用胶头滴管加蒸馏水到标线
D.往容量瓶中转移溶液时应用玻璃棒引流
(4)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是 . ①转移溶液时不慎有少量洒到容量瓶外面
②没有洗涤烧杯和玻璃棒
③定容时俯视刻度线
④容量瓶不干燥,含有少量蒸馏水
⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
⑥未冷却到室温就将溶液转移到容量瓶并定容.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铁与水蒸气反应的说法中不正确的是( )
A. 反应中有氢气产生 B. 此反应需在加热条件下才能发生
C. 生成的铁的化合物中铁全部呈+3价 D. 该反应中水作氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铈是地壳中含量最高的稀土元素,二氧化铈(CeO2)是其重要的化合物。平板液晶显示屏生产过程中产生大量的废玻璃粉末,其中含CeO2、SiO2、Fe2O3等物质,某实验小组以此粉末为原料回收铈,设计流程如图所示:
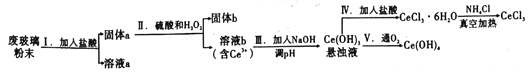
(1)步骤Ⅰ加入过量盐酸后,溶液a中的阳有离子___________________。
(2)步骤Ⅱ中反应的氧化剂和还原剂的物质的量之为___________。
(3)为了使步骤Ⅲ所得悬浊液中的Ce3+浓度为1×10-6mol·L-1,则加入NaOH调节溶液的pH应为____________[已知:Ce(OH)3的Ksp=8.0×10-21,lg2=0.3]。
(4)将NH4Cl固体与CeCl3·6H2O混合真空加热可得无水CeCl3,其中加入NH4Cl的作用是__________。
(5)第Ⅴ步反应的化学方程式是____________________;用反应得到的悬浊液制备纯净的Ce(OH)4需进行的实验操作为______________。
(6)对CeCl3样品纯度进行测定的方法:准确称取样品wg配成100mL溶液,取25.00mL置于锥形瓶中,加入稍过量的过二硫酸铵[(NH4)2S2O8]溶液将Ce3+氧化为Ce4+,然后用萃取剂[用(HT2)表示]萃取Ce4+,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点(其离子反应方程式为Ce4++Fe2+=Ce3++Fe3+),重复2~3次,平均消耗VmL标准溶液。
①“萃取”时存在反应:Ce4++n(HT)2![]() Ce(H2n-4)+4H+,若要提高滴定的准确率,应使溶液呈______性(填“酸”“中”或“碱”)。
Ce(H2n-4)+4H+,若要提高滴定的准确率,应使溶液呈______性(填“酸”“中”或“碱”)。
②经计算,CeCl3样品的纯度为________________。 [M(CeCl3)=246.5g·mol-1]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学键的各种叙述,下列说法中不正确的是( )
A.Ca(OH)2中既有离子键又有共价键
B.在单质或化合物中,一定存在化学键
C.在离子化合物中,可能存在共价键
D.化学反应中肯定有化学键发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.X、Y、Z、W是中学化学中常见的四种气体。己知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石然料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液其有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应;W气体的水溶液滴入酚酞变红色。
请回答下列问题:
(1)X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为_______;
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中有单质生成,该单质应是(填化学式)____________;该反应是氧化还原反应,则其中的氧化剂是(填化学式)_______。
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为________。
(4)检验W气体的方法是_____________。
II.H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,其中生物脱H2S的原理为:
H2S+Fe2(SO4)3=S+2FeSO4+H2SO4
4FeSO4+2H2SO4![]() 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
回答下列方法中的问题。
(l)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是_______。
(2)由图1和图2判断使用硫杆菌的最佳条件为______。若反应温度过高,反应速率下降,其原因是______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“千锤万凿出深山,烈火焚烧若等闲。粉身碎骨浑不怕,只留清白在人间。”明代诗人于谦的《石灰吟》中对“CaCO3→CaO”的转化进行拟人化描述。下列说法正确的是
A. 上述转化属于分解反应 B. 上述转化过程放出大量热
C. 生成的CaO可作氯气的干燥剂 D. CaCO3是水泥的主要成分之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,则下列说法中不正确的是( )
A.标准状况下,a L的氧气和氮气的混合物含有的分子数约为 ![]() ×6.02×1023
×6.02×1023
B.由1L 1 mol?L﹣1的 FeCl3溶液制成的胶体中胶粒总数小于NA个
C.2.3g金属钠变为钠离子失去0.1NA电子
D.2.24L CO2中含有的原子数为3×0.1×6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com