
| A. | 硫离子的核外电子排布式:1s22s22p6 | |
| B. | 碳-14的原子组成符号:${\;}_{6}^{14}$C | |
| C. | 碳原子的外围电子轨道表示式: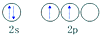 | |
| D. | Cl-的结构示意图: |
分析 A.硫为16号元素,硫离子为硫原子得到2个电子形成,根据核外电子排布规律判断;
B.元素符号的左上角为质量数、左下角为质子数,质量数=质子数+中子数;
C.碳原子最外层为L层,2s、2p轨道各含有2个电子;
D.氯离子核外含有3个电子层,核外电子总数为18.
解答 解:A.S的原子序数为16,硫离子的核外有18电子,根据能量最低原理,其电子排布式为1s22s22p63s23p6,故A错误;
B.碳-14原子的核电荷数=质子数=6,质量数为14,该原子可以表示为614C,故B正确;
C.碳原子价电子为2s、2p,各含有2个分子,碳原子的外围电子轨道表示式: ,故C正确;
,故C正确;
D.Cl-的质子数为17,电子数为18,离子结构示意图为: ,故D正确;
,故D正确;
故选A.
点评 本题考查了化学用语的表示方法判断,题目难度中等,注意掌握核外电子排布式、电子轨道表示式、元素符号等化学用语的表示方法,试题培养了学生灵活应用所学知识的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 无机物 | B. | 有机物 | C. | 盐类 | D. | 非金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3能电离出CO32-,可用澄清石灰水鉴别Na2CO3和NaHCO3溶液 | |
| B. | 钠保存在煤油中,是因为煤油不与钠反应,且钠比煤油密度大、煤油可以隔绝空气 | |
| C. | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应 | |
| D. | 钠长期暴露在空气中的产物是Na2CO3,原因是钠在空气中生成的Na2O会与水和二氧化碳反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阿伏加德罗常数的符号为NA,其近似值为6.02×1023mol-1 | |
| B. | 等物质的量的O2与O3,所含氧原子数相同 | |
| C. | 在0.5molNa2SO4中,含有的Na+数约是6.02×1023 | |
| D. | 化合反应与分解反应可能是氧化还原反应,而复分解反应一定不是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该分子是平面结构 | B. | 该分子是正四面体型 | ||
| C. | 该分子无同分异构体 | D. | 该物质属于卤代烃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com