
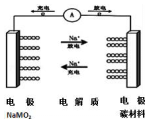
 C-NaMO2����ǿ�ѧ�������з��������ӵ�أ���Ϥ�õ�ؿ��Խ���ͳ﮵�ص�������������7�����õ�صĵ�ط�ӦʽΪ��NaMO2+nC?Na��1-x��MO2+NaxCn�������йظõ�ص�˵����ȷ���ǣ�������
C-NaMO2����ǿ�ѧ�������з��������ӵ�أ���Ϥ�õ�ؿ��Խ���ͳ﮵�ص�������������7�����õ�صĵ�ط�ӦʽΪ��NaMO2+nC?Na��1-x��MO2+NaxCn�������йظõ�ص�˵����ȷ���ǣ�������| A�� | ��طŵ�ʱ����Һ�����������ƶ� | |
| B�� | ��س��ʱ��������ӦʽΪ��nC+x Na+-xe-�TNaxCn | |
| C�� | ������ͬ��������ʱ������������������ӵ����ʵ���������ʱ�� | |
| D�� | �õ�ظ����ĵ缫��ӦΪ��NaMO2-xe-�TNa��1-x��MO2+xNa+ |
���� A��ԭ����У�������е�����������������
B�������У������Ϸ���ʧ���ӵ�������Ӧ��
C����$\frac{m}{M}$��ʧȥ�ĵ�������֪��������ͬ��������ʱ�����������ʱ���������ӵ����ʵ������ƶࣻ
D��ԭ����У���������ʧ���ӵ�������Ӧ��
��� �⣺A����طŵ�ʱ����ԭ��صĹ���ԭ����ԭ����У�������е����������������������������������ƶ�����A����
B����س��ʱ���ǵ���װ�õĹ���ԭ���������Ϸ���ʧ���ӵ�������Ӧ���缫��ӦʽΪNaxCn-xe-�TnC+x Na+����B����
C����Na��Ħ������Ϊ23g/mol����$\frac{m}{M}$��ʧȥ�ĵ�������֪��������ͬ��������ʱ�����������ʱ���������ӵ����ʵ������ƶ࣬��C����
D����طŵ�ʱ����������ʧ���ӵ�������Ӧ����NaMO2-xe-�TNa��1-x��MO2+xNa+����D��ȷ��
��ѡ��D��
���� ���⿼��ѧ��ԭ��غ͵��صĹ���ԭ��֪ʶ��ע����γ�����ڹ���ʱ�ĵ缫��Ӧ������ѶȲ���


 ����������ϵ�д�
����������ϵ�д� �Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
�Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.2mol/L��NaHCO3��Һ�У�c��Na+����c��HCO3-����c��OH-����c��H+����c��CO32-�� | |
| B�� | �����£��������pH=4������ʹ���ϡ�ͳ�pH=5����Һ��������ӵ�ˮ�� | |
| C�� | �����£���ˮ����ε�����������Һ��pH=7������Һ�У�c��NH4+��=c��Cl-�� | |
| D�� | pH=1��NaHSO4��Һ��c��H+��=c��SO42-��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  �������� | B�� |  �������� �������� | C�� |  �������� �������� | D�� |  Ȫˮ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
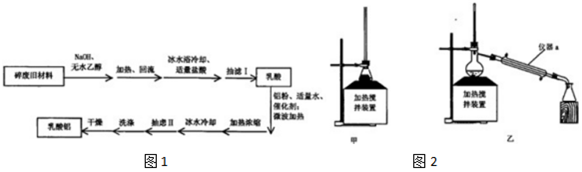
 $��_{��HCl}^{��NaOH}$CH3CH��OH��COOH$\stackrel{Al}{��}$Al[CH3CH��OH��COO]3
$��_{��HCl}^{��NaOH}$CH3CH��OH��COOH$\stackrel{Al}{��}$Al[CH3CH��OH��COO]3| ��� | ʱ��/h | n�����ᣩ��n������ | ?�����ᣩ | ���ʣ�%�� | ��� | ʱ��/h | n�����ᣩ��n������ | ?�����ᣩ | ���ʣ�%�� |
| 1 | 8 | 3.025 | 0.10 | 64.0 | 4 | 10 | 2.935 | 0.20 | 78.4 |
| 2 | 8 | 3.025 | 0.20 | 72.0 | 5 | 10 | 3.025 | 0.20 | 90.2 |
| 3 | 8 | 3.025 | 0.30 | 68.5 | 6 | 10 | 3.505 | 0.20 | 91.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������A��B�������ֱ���ȫȼ�պ����ɵ�CO2�����ĵ�O2�����ʵ�������ͬ����A��Bһ����Ϊͬϵ�� | |
| B�� | �е�Ƚϣ������飾�����飾������ | |
| C�� | �������Ҵ���һ�������·�Ӧ��������������ˮ�ķ�Ӧ����ȡ����Ӧ | |
| D�� | �жϱ������в�����̼̼������̼̼˫���Ľ���ṹ�������ǣ��ڶ��ױ�ֻ��һ�ֽṹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֬�������������������࣬������ͬϵ�� | |
| B�� | �������һ�ȴ�����5�� | |
| C�� | ͼ�� ��̪�����е������������ܹ�ƽ�� ��̪�����е������������ܹ�ƽ�� | |
| D�� | ij�л�����ȫȼ�����ɵ����ʵ�����CO2��H2O�����л���ķ���ʽһ��ΪCnH2n |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
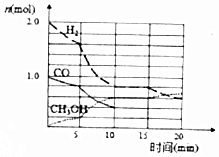 ��ҵȼ��ú��ʯ�͵Ȼ�ʯȼ���ͷų�����NOx��CO��CO2�����壬������Ⱦ�������Է���������������̼�ȴ�����ʵ����ɫ�������������ã�
��ҵȼ��ú��ʯ�͵Ȼ�ʯȼ���ͷų�����NOx��CO��CO2�����壬������Ⱦ�������Է���������������̼�ȴ�����ʵ����ɫ�������������ã�| ���� | �� | �� |
| ��Ӧ��Ͷ���� | 1mol CO2��3molH2 | amol CO2��3amolH2 bmolCH3OH��g����bmolH2O��g�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ۢ� | B�� | �٢ڢۢ� | C�� | �ڢۢ� | D�� | ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʵ����������ʵ����� | |
| B�� | ���ʵ����������ʵ�Ħ������ | |
| C�� | ���ʵ�������������������Ŀ�Ķ��� | |
| D�� | ���ʵ�����һ�ֻ��������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com