
| A. | 原子半径:W>Z>Y>X>M | |
| B. | XZ2、X2M4均为直线形的共价化合物 | |
| C. | W2Z2是既含离子键又含共价键的离子化合物 | |
| D. | 由X、Y、Z、M四种元素形成的化合物一定既有离子键、又有共价键 |
分析 X、Y、Z、M、W为五种短周期元素,Y与M形成的气态化合物在标准状况下的密度为0.76g•L -1,该化合物的摩尔质量为0.76g•L -1×22.4L/mol=17g/mol,考虑为NH3,X、Y、Z是原子序数依次递增的同周期元素,故Y为N元素,M为H元素.X与Z可形成XZ2分子,则X位于偶数族,X、Y、Z原子最外层电子数之和为15,故X、Z的最外层电子数之和为15-5=10,Z最外层电子数为偶数,二者平均最外层电子数为5,故Z处于第ⅥA族,X处于第ⅣA族,所以X为C元素,Z为O元素;W的质子数是X、Y、Z、M四种元素质子数之和的$\frac{1}{2}$,推出W的质子数为$\frac{1}{2}$(6+7+8+1)=11,所以W为Na元素,据此解答.
解答 解:X、Y、Z、M、W为五种短周期元素,Y与M形成的气态化合物在标准状况下的密度为0.76g•L -1,该化合物的摩尔质量为0.76g•L -1×22.4L/mol=17g/mol,考虑为NH3,X、Y、Z是原子序数依次递增的同周期元素,故Y为N元素,M为H元素.X与Z可形成XZ2分子,则X位于偶数族,X、Y、Z原子最外层电子数之和为15,故X、Z的最外层电子数之和为15-5=10,Z最外层电子数为偶数,二者平均最外层电子数为5,故Z处于第ⅥA族,X处于第ⅣA族,所以X为C元素,Z为O元素;W的质子数是X、Y、Z、M四种元素质子数之和的$\frac{1}{2}$,推出W的质子数为$\frac{1}{2}$(6+7+8+1)=11,所以W为Na元素.
A.同周期自左向右原子半径减小,同主族自上到下原子半径增大,故原子半径Na>C>N>O>H,即W>X>Y>Z>M,故A错误;
B.CO2为直线型共价化合物,但C2H4为平面形共价化合物,故B错误;
C.Na2O2为离子化合物,含有离子键、共价键,故C正确;
D.由C、N、O、H四种元素形成的化合物不一定既有离子键,又有共价键,如(NH2)2CO中只含共价键,故D错误,
故选C.
点评 本题考查结构性质位置关系综合应用,推断元素是解题关键,根据密度判断Y与M形成的气态化合物是氨气是推断的关键,注意X、Z元素推断奇偶性的利用.


科目:高中化学 来源: 题型:选择题
| A. | 用食醋蒸熏对房间消毒杀菌 | |
| B. | SO2通入品红中溶液变为无色 | |
| C. | 红糖水中加入活性炭溶液变为无色 | |
| D. | 少量胆矾粉末加入到浓硫酸中固体变白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
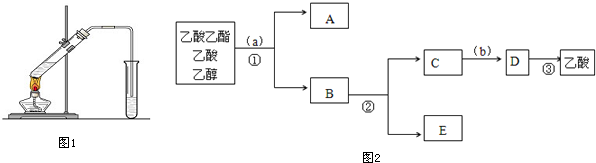
 $\stackrel{反应1}{→}$X$\stackrel{反应2}{→}$Y$\stackrel{反应3}{→}$
$\stackrel{反应1}{→}$X$\stackrel{反应2}{→}$Y$\stackrel{反应3}{→}$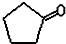
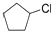
 .
.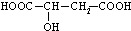
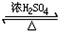 CH3CH2OOC-CHOH-CH2COOCH2CH3+2H2O
CH3CH2OOC-CHOH-CH2COOCH2CH3+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:填空题
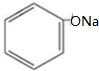 +CO2+H2O→
+CO2+H2O→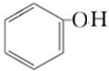 +NaHCO3.
+NaHCO3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CH3COOC2H5+H2O.其中浓H2SO4的作用是催化剂和吸水剂
CH3COOC2H5+H2O.其中浓H2SO4的作用是催化剂和吸水剂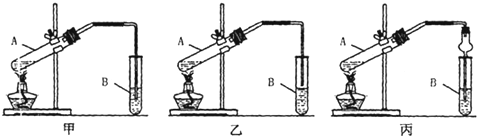
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甘油和水、乙醛和水、乙酸和乙醇 | |
| B. | 油酸和水、甲苯和水、己烷和苯 | |
| C. | 乙酸乙酯和水、酒精和水、苯酚和水 | |
| D. | 二溴乙烷和水、溴苯和水、硝基苯和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 饱和Na2CO3溶液 | B. | CaCl2溶液 | C. | Na2SiO3溶液 | D. | Ca(ClO)2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com