
| A. | 1mol金属钠与足量氧气反应转移的电子数为NA | |
| B. | 标准状况下,22.4L甲苯中含C-H键数目为8NA | |
| C. | 标准状况下,11.2L氦气中含有0.5NA个氦原子 | |
| D. | 常温常压下,含有NA个氮气和乙烯分子的混合气体质量为28g |
分析 A、钠和氧气反应后变为+1价;
B、标况下甲苯为液体;
C、求出氦气的物质的量,然后根据氦气为单原子分子来分析;
D、氮气和乙烯的相对分子质量均为28g/mol.
解答 解:A、钠和氧气反应后变为+1价,故1mol钠反应后转移NA个电子,故A正确;
B、标况下甲苯为液体,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、标况下11.2L氦气的物质的量为0.5mol,而氦气为单原子分子,故0.5mol氦气中含0.5NA个原子,故C正确;
D、氮气和乙烯的相对分子质量均为28g/mol,故NA个氮气和乙烯分子的物质的量为1mol,故质量为28g,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
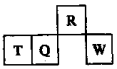 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中W所处的周期序数是最外层电子数的一半.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中W所处的周期序数是最外层电子数的一半.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 含T的盐溶液一定显酸性 | |
| D. | 实验室制备T的氢氧化物可以通过R形成的氢化物通入到T离子的溶液中得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
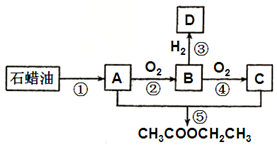 烃A是一种重要的化工原料.已知A在标准状况下的密度为1.25g•L-1,B可发生银镜反应.它们之间的转化关系如图:
烃A是一种重要的化工原料.已知A在标准状况下的密度为1.25g•L-1,B可发生银镜反应.它们之间的转化关系如图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Cu+O2?2CuO | B. | CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O | ||
| C. | 2KClO3?2KCl+3O2↑ | D. | CaCO3+2HCl═CaCl2+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 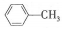 的一溴代物和 的一溴代物和 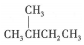 的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) | |
| B. | CH3CH=CHCH3分子中的四个碳原子在同一直线上 | |
| C. | 按系统命名法,化合物 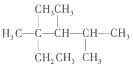 的名称是2,3,4-三甲基-2-乙基戊烷 的名称是2,3,4-三甲基-2-乙基戊烷 | |
| D. | 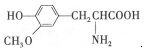 与 与 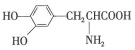 都是α-氨基酸且互为同系物 都是α-氨基酸且互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④>③>①>② | B. | ②>③>①=④ | C. | ②>③>①>④ | D. | ③>②>①=④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2009年12月在哥本哈根召开的国际气候会议受到全球政要的广泛关注.减缓工业生产大量二氧化硫的排放以抑制全球气候变暖成为该会议的主题 | |
| B. | 针对目前甲型H1N1流感的扩散情况,要加强对环境、个人的消毒预防.其中消毒剂常选用含氯消毒剂、酒精、双氧水等适宜的物质 | |
| C. | 2009年诺贝尔物理学奖授予华裔科学家高锟,是因其在光纤材料领域取得了卓越贡献.光纤的主要成分与玛瑙相同,通常情况下不与强氧化剂和强酸反应 | |
| D. | 建国60周年庆典晚会上,天安门广场燃放的焰火是某些金属元素魅力的展现 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
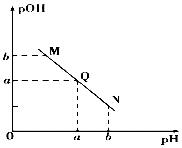 现有①0.1mol/L NaOH溶液和②0.1mol/L HX溶液.
现有①0.1mol/L NaOH溶液和②0.1mol/L HX溶液.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com