
 M��OH��2
M��OH��2  2H++MO22-
2H++MO22-| 1 |
| 10 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
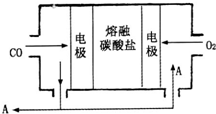 ��2013?����ģ�⣩�Ƽ��仯������й㷺����;��
��2013?����ģ�⣩�Ƽ��仯������й㷺����;��
| ||
| ||
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| ���� | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
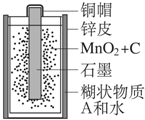 �Ͼɸɵ�������������ǿ��Ի������õģ�ij���ͺŸɵ�ص�������ͼ��ʾ����ش��������⣺
�Ͼɸɵ�������������ǿ��Ի������õģ�ij���ͺŸɵ�ص�������ͼ��ʾ����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
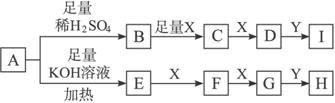
��1��A���ʵĻ�ѧʽΪ____________________��
��2����Y��__________����I��H��Һ���������ڣ���ᡱ������Ρ����������__________�ࡣ
��3��д����������ת���Ļ�ѧ����ʽ��
B��C________________________________________________________________��
E��F_________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

��ش��������⣺
(1)A���ʵĻ�ѧʽΪ__________��H���ʵ�����Ϊ__________��
(2)G![]() J�Ļ�ѧ����ʽΪ_________________________________________________��
J�Ļ�ѧ����ʽΪ_________________________________________________��
(3)D����������ǡ�÷�Ӧ�����ӷ���ʽΪ______________��������Һ�����Ե�ԭ����______________________________________(�����ӷ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com