
����Ŀ��[���ʽṹ������]
��֪������ͭ��Һ�е��백�������ƣ�H2N��CH2��COONa�����ɵõ������A����ṹ��ͼ1��
��1��CuԪ�ػ�̬ԭ�ӵ���Χ�����Ų�ʽΪ ��
��2��Ԫ��C��N��O�ĵ�һ�������ɴ�С����˳��Ϊ ��
��3�������A��̼ԭ�ӵĹ���ӻ�����Ϊ ��
��4��1mol���������ƣ�H2N��CH2��COONa�����ЦҼ�����ĿΪ ��
��5�����������Ʒֽ����֮һΪ������̼��д��������̼��һ�ֵȵ����壺��д��ѧʽ����
��6����֪������ͭ���տ�������һ�ֺ�ɫ���壬��ṹ��ͼ2����û�����Ļ�ѧʽ�� ��
���𰸡�
��1��3d104s1
��2��N��O��C
��3��sp3��sp2
��4��8mol
��5��N2O����SCN����N3���ȣ�
��6��Cu2O
���������⣺��1��Cu��29��Ԫ�أ���ԭ�Ӻ�����29�����ӣ�3d�ܼ�����10�����ӡ�4s�ܼ�����1�����ӣ�3d��4s�ܼ��ϵ���Ϊ����Χ���ӣ����ݹ���ԭ��֪���̬ԭ����Χ�����Ų�ʽΪ3d104s1��
���Դ��ǣ�3d104s1��
��2��ͬ���ڴ����ң�Ԫ�صĵ�һ�����ܳ��������ƣ���NԪ��ԭ�ӵ�2p�ܼ����ڰ����ȶ�״̬�������ϵͣ���һ�����ܸ���ͬ�������ڵ�Ԫ�أ�����C��N��O����Ԫ�صĵ�һ����������С���������˳����N��O��C��
���Դ��ǣ�N��O��C��
��3�������A������һ��̼��C=O��̼���ӻ���ʽΪsp2�ӻ�����һ��̼��Χ���ǵ�����̼���ӻ���ʽΪsp3�ӻ���
���Դ��ǣ�sp3��sp2��
��4�����۵���Ϊ�Ҽ�������˫����һ���ǦҼ�һ���Ǧм���H2N��CH2��COONa�к���8���Ҽ�������1mol�����������к��ЦҼ�����ĿΪ8mol��
���Դ��ǣ�8mol��
��5��һ��������̼������ԭ�Ӹ���Ϊ3�����۵�����Ϊ16��ԭ�Ӹ�����ȡ��۵�������ȵ���Ϊ�ȵ����壬��CO2�ĵȵ�����Ϊ��N2O����SCN����N3���ȣ���
���Դ��ǣ�N2O����SCN����N3���ȣ���
��6�����þ�̯��֪���û�������Oԭ�Ӹ���=1+8�� ![]() =2��Cuԭ�Ӹ���=4��ͭԭ�Ӻ���ԭ�Ӹ���֮��=4��2=2��1�������仯ѧʽΪ��Cu2O��
=2��Cuԭ�Ӹ���=4��ͭԭ�Ӻ���ԭ�Ӹ���֮��=4��2=2��1�������仯ѧʽΪ��Cu2O��
���Դ��ǣ�Cu2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У����ڵ���ʲ��ڴ�״̬���ܵ�����ǣ� ��
A.����B.����C.����D.Һ̬�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��һ�ֳ����Ľ������ʣ�B �ǵ���ɫ���壬����ת����ϵͼ�ж�����˵����ȷ���ǣ� ��
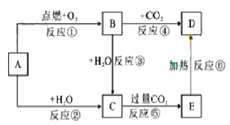
A. A������������������һ�ֳ���������F��B��F���������������ӵ���Ŀ�ȷֱ���1��1��1��2
B. ��ȫȼ��Wg��CO��H2�Ļ�����壬Ȼ�����������B��Ӧ�����������С��Wg
C. ��ͬ�¶��£��ֱ���ʢ������0.1mol/LD��E��Һ����֧�Թ��е���2�η�̪��Һ����ʢ��D����Һ���Թ��к�ɫ����
D. �ýྻ�IJ�˿պȡij����Һ�����ڻ��������գ�����ɫ�ܲ����ܹ۲쵽���� ����ɫ������Һ��һ�����м����ӣ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��ҵ��ˮ�п��ܺ���Na+��Mg2+��Al3+��Cl-��SO42-�еļ������ӡ�
a��ȡ�����÷�ˮ���Թ��У�����������Ba(NO3)2��Һ��ϡ���ᣬ������ɫ��������ַ�Ӧ����ˣ�����Һ�м���AgNO3��Һ����������
b����ȡ10mL�÷�ˮ���Թ��У��μ�NaOH��Һ�Ȳ�����ɫ�������ֳ����ܽ⡣���ɳ��������ʵ��������NaOH�����ʵ�����ϵ����ͼ��ʾ��
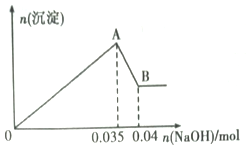
��������ʵ���ͼ�����ݣ�
��1���÷�ˮ��һ�������е�������______________________________(�����ӷ���)��
��2��д��A��B�����з�����Ӧ�����ӷ���ʽ��________________________��
��3���÷�ˮ�У�c(Al3+)=______________��
��4����ʵ��������100mL2mol/L��NaOH��Һʱ���õ��IJ����������ձ�������������Ͳ�⣬����Ҫ_________(����������)��
�����в���ʹ������ҺŨ��ƫ�����(��д��ĸ)_________��
A�������������������
B����NaOH����ֽ���ϳ���
C��NaOH���ձ����ܽ��δ��ȴ������ת�Ƶ�����ƿ��
D��������ƿת��ʱ��������Һ�����
E��δϴ���ܽ�NaOH���ձ�
F������ʱ���ӿ̶���
G������ƿδ���T����������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���� NaCl ��Һ�����ΪV mL���ܶ�Ϊ�� g/cm3 �� ��������Ϊ w%�����ʵ���Ũ��Ϊc mol/L����Һ�к�NaCl������Ϊm g��
��1����m��V��ʾ��Һ���ʵ���Ũ�� ��
��2����w���ѱ�ʾ��Һ���ʵ���Ũ�� ��
��3����c���ѱ�ʾ��Һ���������� ��
��4����w��ʾ���¶���NaCl���ܽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҩ���й������Ĵ�����֮һ����Զֵ�������セ����Ҳ��Զ�ἤ��������ȥ�ܷ�ͼǿ���ڻ�ҩ�ڷ�����ըʱ���������µķ�Ӧ��KNO3+C��S===K2S+NO2��+CO2��(δ��ƽ����������������______________________�� ����������______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����±仯����Ҫ���뻹ԭ������ʵ�ֵ����� ��
A. Cl-��Cl2 B. SO42-��BaSO4 C. Cu��Cu2+ D. MnO4-��Mn2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʲ�����Ư���Ե��ǣ� ��
A.�������B.��84������ҺC.����D.������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����mgþ�����Ļ�����м���������ϡ���ᣬǡ����ȫ��Ӧ���ɱ�״���µ�����bL����Ӧ�����Һ�м���cmol/L����������ҺVmL��ʹ�������Ӹպó�����ȫ���õ��ij�������Ϊng���ٽ��õ��ij����������������ٸı�Ϊֹ���õ�����pg�������й�ϵ����ȷ���ǣ� ��
A. n��17Vc��m B. 5m/3��p��17m/9
C. p��m+cV/125 D. c=1000b/11.2V
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com