
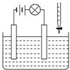
 测定电解质溶液导电性的实验装置如图所示,向1mol?L-1氢氧化钡溶液中逐滴加入下列溶液,灯泡不是由亮→暗→亮的是( )
测定电解质溶液导电性的实验装置如图所示,向1mol?L-1氢氧化钡溶液中逐滴加入下列溶液,灯泡不是由亮→暗→亮的是( )| A、12 mol?L-1的浓盐酸 |
| B、硫酸铜溶液 |
| C、硫酸镁溶液 |
| D、稀硫酸 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(1)(4)(6)(7) |
| B、(4)(6)(9)(10) |
| C、(3)(5)(6)(8) |
| D、(5)(6)(8)(9) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、改变压强,平衡不发生移动,反应放出的热量不变 |
| B、若在原电池中进行,反应放出的热量不变 |
| C、升高温度,反应速率加快,反应放出的热量不变 |
| D、加入催化剂,改变了反应的途径,也改变了反应的△H |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径 |
| B、废旧电池不能随意丢弃,要进行深埋处理,防止重金属污染 |
| C、Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
| D、据测定,许多反应的温度每升高10℃,其反应速率增加2~4倍.在实验室或工业生产中,常采用加热的方法使化学反应在较高的温度下进行,以提高反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4Fe(OH)2+2H2O+O2=4Fe(OH)3↓ |
| B、2Fe+2H2O+O2=2Fe(OH)2↓ |
| C、2H2O+O2+4e-=4OH- |
| D、Fe-3e-=Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe+H2SO4=FeSO4+H2↑ |
| B、CO+CuO═Cu+CO2↑ |
| C、Cu2(OH)2CO3═2CuO+H2O+CO2↑ |
| D、4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用稀硫酸清洗做焰色反应的铂丝 |
| B、用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |
| C、用100mL容量瓶配制50mL 0.1 mol?L-1的盐酸 |
| D、测NaOH熔点时可以将NaOH放入石英坩埚中高温熔化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com