与54g水所含原子总数相同的固态碘是______mol;同温同压下,同质量的氯气和二氧化碳气体的体积比为______.
【答案】
分析:计算出54g水的物质的量,进而计算原子的物质的量,根据原子的物质的量相等可计算出碘的物质的量;
根据质量计算出气体的物质的量,气体的体积之比等于物质的量之比.
解答:解:54g水的物质的量为n=
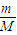
=
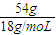
=3mol,
原子的物质的量为3×3mol=9mol,
固态碘与水的原子个数相等,则原子的物质的量相等,
即n(I)=9mol,
则n(I
2)=4.5mol;
设氯气和二氧化碳的质量分别为1g,则物质的量分别为n(Cl
2)=
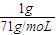
=
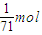
,n(CO
2)=
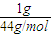
=
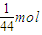
,
在相同条件下,气体的体积之比等于物质的量之比,
所以V(Cl
2):V(CO
2)=n(Cl
2):n(CO
2)=
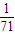
:
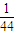
=44:71,
故答案为:4.5mol;44:71.
点评:本题考查物质的量的有关计算,题目难度不大,注意物质的量与质量、体积之间计算公式的运用.

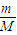 =
=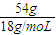 =3mol,
=3mol,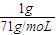 =
=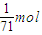 ,n(CO2)=
,n(CO2)=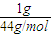 =
=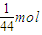 ,
,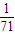 :
: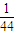 =44:71,
=44:71,

 阅读快车系列答案
阅读快车系列答案