
某醇在适当条件下与足量的乙酸发生酯化,得到的酯的相对分子质量a与原来醇的相对分子量b的关系是a=b+84,有关该醇应该具有的结构特点的描述正确的是()
A. 该醇分子中一定具有甲基
B. 该醇分子中一定没有甲基
C. 该醇分子中至少含有三个碳原子
D. 该醇分子中具有两个醇羟基
考点: 有机物的推断;醇类简介.
专题: 有机物分子组成通式的应用规律.
分析: 醇与足量的乙酸反应生成酯,设醇中羟基数目为n,则Mr(醇)+n×Mr(乙酸)=Mr(酯)+n×Mr(水),故Mr(酯)﹣Mr(醇)=n×Mr(乙酸)﹣n×Mr(水)=84,即60n﹣18n=84,解得n=2,据此解答.
解答: 解:醇与足量的乙酸反应生成酯,设醇中羟基数目为n,则Mr(醇)+n×Mr(乙酸)=Mr(酯)+n×Mr(水),故Mr(酯)﹣Mr(醇)=n×Mr(乙酸)﹣n×Mr(水)=84,即60n﹣18n=84,解得n=2,
由于2个﹣OH连接在同一碳原子上,不稳定,故该醇分子至少有2个C原子,该醇分子中含有2个﹣OH,故该醇分子中可能含有甲基、也可能没有甲基,综上分析,选项ABC错误,D正确,故选D.
点评: 本题考查有机物推断,根据酯化反应特点,利用质量守恒确定醇中羟基数目是关键,侧重考查学生对数据的分析处理能力,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
向10mL pH=12的NaOH溶液中加入10mL某酸,再滴入几滴甲基橙,溶液呈红色,则这种酸可能是()
A. pH=2的硫酸 B. 0.01 mol•L﹣1的甲酸
C. pH=2的醋酸 D. 0.01 mol•L﹣1的硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
以下有关原子结构及元素周期律的叙述正确的是( )
A.第ⅠA族元素铯的两种同位素137Cs比133Cs多4个质子
B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小
C.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强
D.同主族元素从上到下,单质的熔点逐渐降低
查看答案和解析>>
科目:高中化学 来源: 题型:
环境保护正日益受到政府和社会公众的重视,下列污染中,已成为我国必须治理的有 ( )。
①废弃塑料制品造成的“白色污染” ②排放含有机物和含磷(Na5P3O4)洗
衣粉污水造成的水质污染 ③机动车辆排放的尾气(NOx、CO等)引起的光
化学污染 ④燃烧煤、石油等化石燃料放出的二氧化硫和粉尘、空气污染和
酸雨 ⑤冰箱、空调等泄漏出的制冷剂(如氟利昂)破坏臭氧层
A.①②③④⑤ B.①②③
C.①② D.①
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有机物中加入溴水,充分振荡后静置,观察到水层变为无色,有机溶液层为橙黄色,该有机物是()
A. 乙醛 B. 1﹣己烯 C. 1,3﹣丁二烯 D. 苯
查看答案和解析>>
科目:高中化学 来源: 题型:
在同温同压下,一定量的某有机物和过量的金属钠反应产生a L氢气,另取等量的该有机物与足量的小苏打溶液反应,可以收集二氧化碳气体b L,若a=b,则该有机物可能是()
A. HOOC﹣COOH B. HOOC﹣CH2CH2OH
C. HOCH2﹣CH2OH D. CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细。由此判断表中所列M、N、P物质,其中可以成立的是( )
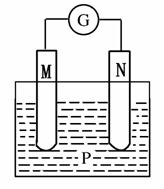
| 选项 | M | N | P |
| A | Zn | Cu | 稀H2SO4溶液 |
| B | Cu | Fe | 稀HCl溶液 |
| C | Ag | Zn | AgNO3溶液 |
| D | Zn | Fe | FeSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学按图所示的装置进行电解实验.下列说法正确的是()
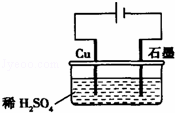
A. 电解过程中,铜电极上有H2产生
B. 电解初期,主要反应方程式为:Cu+H2SO4 CuSO4+H2↑
CuSO4+H2↑
C. 电解一定时间后,石墨电极上有铜析出
D. 整个电解过程中,H+的浓度不断增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com