
 氯酸钠(NaClO3)是无机盐工业的重要产品之一.
氯酸钠(NaClO3)是无机盐工业的重要产品之一.分析 (1)石灰乳与氯气反应生成氯化钙和氯酸钙,除去氯化钙后,可加入碳酸钠溶液,以生成碳酸钙沉淀,以此得到氯酸钠;
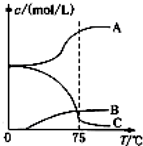
(2)氯气与氢氧化钠反应温度低时生成NaClO,温度高时生成NaC1O3,据此分析;
(3)采用无隔膜电解饱和食盐水法生产氯酸钠,同时在阴极生成氢气;
(4)①酸性条件下,亚铁离子被ClO3-氧化为铁离子,自身被还原为氯离子;静置10min可以使反应进行完全;
②K2Cr2O7溶液具有强氧化性,能腐蚀碱式滴定管的橡胶管;
③滴定实验操作一般重复2-3次;
(5)如果溶液中的Fe2+被空气中的氧气,在滴定时消耗的(NH4)2Fe(SO4)2溶液会偏多.
解答 解:热的石灰乳通入氯气,反应的方程式为:2Cl2+2Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+Ca(ClO)2+2H2O,除去CaCl2后主要成分为Ca(ClO)2,要加入钠盐得到NaClO3,应加入Na2CO3,发生复分解反应生成碳酸钙沉淀,
故答案为:Na2CO3;
(2)氯气与氢氧化钠反应温度低时生成NaClO,温度高时生成NaC1O3,图中C的浓度随着温度的升高而减小,所以C代表ClO-;
故答案为:ClO-;
(3)采用无隔膜电解饱和食盐水法生产氯酸钠,同时在阴极生成氢气,其反应的方程式为:NaC1+3H2O$\frac{\underline{\;通电\;}}{\;}$NaC1O3+3H2↑;
故答案为:NaC1+3H2O$\frac{\underline{\;通电\;}}{\;}$NaC1O3+3H2↑;
(4)①酸性条件下,亚铁离子被ClO3-氧化为铁离子,自身被还原为氯离子,其反应的离子方程式为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;静置10min可以使亚铁离子和ClO3-充分反应;
故答案为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;使溶液中C1O3-与Fe2+反应充分完全;
②K2Cr2O7溶液具有强氧化性,能腐蚀碱式滴定管的橡胶管,所以应该用酸式滴定管盛放;
故答案为:酸式滴定管;
③为精确测定样品中C1O3-的质量分数,滴定实验操作一般重复2-3次,即重复上述步骤2、3操作2-3次;
故答案为:重复上述步骤2、3操作2-3次;
(5)如果溶液中的Fe2+被空气中的氧气,则溶液中Fe2+的浓度会减小,在滴定时消耗的(NH4)2Fe(SO4)2溶液的体积会偏大,所以测定的结果偏高;故答案为:溶液中的Fe2+被空气中的氧气氧化.
点评 本题以氯酸盐的制备为载体考查物质的分离、提纯以及含量的测定、氧化还原反应滴定法的应用等,侧重于学生的分析、实验能力的考查,注意把握物质的性质为解答该题的关键,题目难度中等.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:解答题
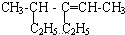 4-甲基-3-乙基-2-己烯
4-甲基-3-乙基-2-己烯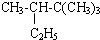 2,2,3一三甲基戊烷
2,2,3一三甲基戊烷 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将固体加入容量瓶中溶解并稀释至刻度线,配制成一定物质的量浓度的溶液 | |
| B. | 稀释硫酸时,往装有浓硫酸的烧杯中注入水 | |
| C. | 用托盘天平称取10.600 g的Na2CO3固体,溶于1 L的水可配成0.1 mol/L的溶液 | |
| D. | 容量瓶中残留少量蒸馏水时,无需干燥,对配制的结果没有影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 阴极发生还原反应,其电极反应式:Ni2++2e-═Ni | |
| B. | 电解过程中,阳极质量的减少与阴极质量的增加相等 | |
| C. | 电解后,电解槽底部的阳极泥中只有Cu和Pt | |
| D. | 电解后,溶液中存在的阳离子只有Fe2+和Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 黑火药是我国古代四大发明之一,配方为“一硫二硝三木炭”,其中的硝是指硝酸 | |
| B. | 包装食品里常有硅胶、生石灰、还原铁粉三类小包,其作用相同 | |
| C. | 洪灾区民众用明矾净水并用漂白粉消毒,二者化学原理相同 | |
| D. | 家中做卫生保洁时,不可将“84”消毒液与洁厕精(含浓盐酸)混合使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com