
(2011?连云港模拟)短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示.下列说法正确的是( )
| ||||||||||||||||||


科目:高中化学 来源: 题型:阅读理解
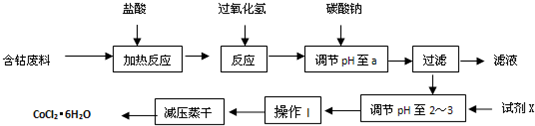
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 | 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (2011?连云港模拟)某化学兴趣小组的同学用如图所示装置研究电化学问题.当闭合该装置的电键时,观察到电流计的指针发生偏转.下列有关说法不正确的是( )
(2011?连云港模拟)某化学兴趣小组的同学用如图所示装置研究电化学问题.当闭合该装置的电键时,观察到电流计的指针发生偏转.下列有关说法不正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
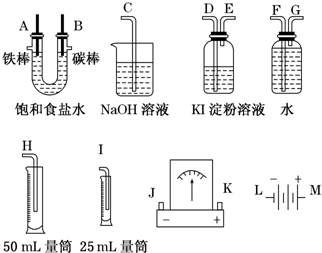
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com