
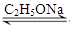 CH3COCH2COOC2H5��C2H5OH����Ӧ�д����Ҵ������ɽ����ƺͲ��������������е����Ҵ��������ɵģ���һ����Ӧ��ʼ�����ɵ��Ҵ��ֻ�������Ʒ�Ӧ�����Ҵ��ơ��������������Ʊ����������£�
CH3COCH2COOC2H5��C2H5OH����Ӧ�д����Ҵ������ɽ����ƺͲ��������������е����Ҵ��������ɵģ���һ����Ӧ��ʼ�����ɵ��Ҵ��ֻ�������Ʒ�Ӧ�����Ҵ��ơ��������������Ʊ����������£�
| | �� | �� | �ױ� | �Զ��ױ� | ���Ȼ�̼ |
| �ܶȣ�g/cm3�� | 0.97 | 0.88 | 0.87 | 0.86 | 1.60 |
| �۵㣨�棩 | 97.8 | 5.5 | -95 | 13.3 | -22.8 |
| �е㣨�棩 | 881.4 | 80 | 111 | 138. 4 | 76.8 |
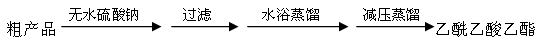


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
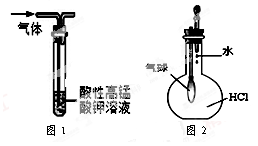
| A���ø���pH��ֽ�ⶨij������ˮ��pH |
| B����ͼ1װ���ܳ�ȥSO2�л��е�CO2 |
| C����ͼ2װ������֤HCl������ˮ�е��ܽ��� |
| D����25 mL��ʽ�ζ�����ȡ20.00 mLKMnO4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2Ca2����2K����Mg2����4
2Ca2����2K����Mg2����4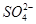 ��2H2O
��2H2O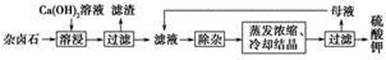
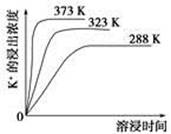
 ?
? CaCO3(s)��
CaCO3(s)��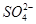
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������AgNO3��Һ�а�ɫ�������� |
| B������ϡ��������ɫ��ζ����������������ʹ�����ʯ��ˮ����� |
| C������MgCl2��Һ�а�ɫ�����������ټ���ϡ��������ܽ⣬��������ʹ����ʯ��ˮ����ǵ���ɫ��ζ���� |
| D������Ba(OH)2��Һ�а�ɫ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������̼������Һ�����ˣ���ȥ��������Һ�в����������� |
| B����������������Һ�����ˣ���ȥ��������Һ�в����������� |
| C�����������������Һ�����ˣ���ȥ��������Һ�в����������� |
| D���������̼�����Һ�����ˣ���ȥ��������Һ�в����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
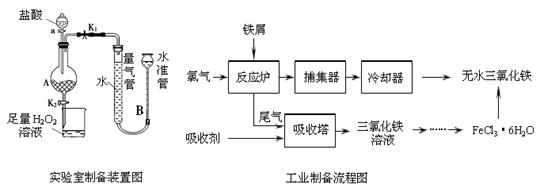
| �¶�/�� | 0 | 20 | 80 | 100 |
| �ܽ��(g/100 g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
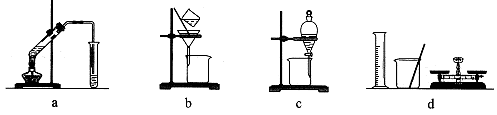
| A��a�飺�Ʊ������������� |
| B��b�飺��ȥ����ˮ�е���ɳ |
| C��c�飺��CCl4��ȡ��ˮ�еĵ� |
| D��d�飺����100 mL 1.00 mol/L NaCl��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ij����ͨ��Ʒ����Һ�У�Ʒ����ɫ��˵��������һ����SO2 |
| B���ò�˿պȡij��Һ������ɫ��Ӧ������ʻ�ɫ��˵������Һһ��������K�� |
| C������һ��ǿ������������Һ�����������ġ�ͨ·����˵������һ��������ˮ�� |
| D����X����Һ�м���������Һ��ˮԡ���ȣ�����������˵��X��һ������ȩ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
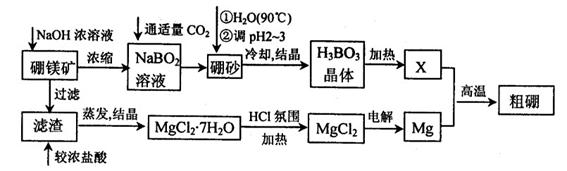
 10-12������ҺpH=6ʱ (��С���û�С�)Mg(OH)2����������
10-12������ҺpH=6ʱ (��С���û�С�)Mg(OH)2�����������鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com