
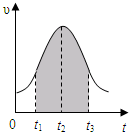
 ʵ����0.01mol/L��KMnO4��������Һ��0.1mol/L��H2C2O4��Һ�������Ϻ�Ӧ���ʦ�[mol/��L?s��]�뷴Ӧʱ��t��s���Ĺ�ϵ��ͼ��ʾ���÷�Ӧ�Ļ�ѧ����ʽΪ��2KMnO4+5H2C2O4+3H2SO4�TK2SO4+2MnSO4+10CO2��+8H2O
ʵ����0.01mol/L��KMnO4��������Һ��0.1mol/L��H2C2O4��Һ�������Ϻ�Ӧ���ʦ�[mol/��L?s��]�뷴Ӧʱ��t��s���Ĺ�ϵ��ͼ��ʾ���÷�Ӧ�Ļ�ѧ����ʽΪ��2KMnO4+5H2C2O4+3H2SO4�TK2SO4+2MnSO4+10CO2��+8H2O| ��c |
| ��t |
| ��c |
| ��t |


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������NaI����ɫ����Һ��K+��Ba2+��OH-��MnO4- |
| B��1.2mol/L CaCl2��Һ��NH4+��SO42-��Na+��NO3- |
| C����ʹ��ɫʯ����Һ����ɫ����Һ��Ba2+��NO3-��NH4+��SO32- |
| D����������ΪKHSO4����Һ��Fe2+��Mg2+��NO3-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ�����ᷴӦ |
| B���������Һ�м�������NaOH��Һ |
| C��ϡ������Ba��OH��2��Һ��Ӧ |
| D��NaOH��Һ��ϡ���ᷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ۢ� | B���ڢܢ� |
| C���٢ڢ� | D���٢ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 һ���¶��£���һ�̶�����������У�ͨ��һ������CO��H2O���������·�Ӧ��CO ��g�� ʮH2O ��g��?CO2��g�� ʮ H2 ��g������H��0
һ���¶��£���һ�̶�����������У�ͨ��һ������CO��H2O���������·�Ӧ��CO ��g�� ʮH2O ��g��?CO2��g�� ʮ H2 ��g������H��0| ʱ�䣨min�� | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
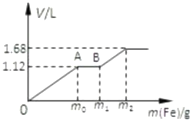 ��50mLϡH2SO4��ϡHNO3�Ļ����Һ���������ۣ�����������۵����������������������״����֮��Ĺ�ϵ��ͼ��ʾ����ÿһ��ֻ��Ӧһ����Ӧ��
��50mLϡH2SO4��ϡHNO3�Ļ����Һ���������ۣ�����������۵����������������������״����֮��Ĺ�ϵ��ͼ��ʾ����ÿһ��ֻ��Ӧһ����Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
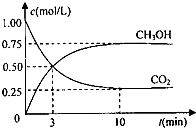 Ϊʵ�֡����ܼ��š��͡���̼���á���һ���������ν�CO2ת��Ϊ��������Դ��
Ϊʵ�֡����ܼ��š��͡���̼���á���һ���������ν�CO2ת��Ϊ��������Դ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com