
 为检验精盐纯度,需要配制240mL 1mol/L NaCl(精盐)溶液.
为检验精盐纯度,需要配制240mL 1mol/L NaCl(精盐)溶液.| n |
| V |
| n |
| V |
| n |
| V |
| n |
| V |
| n |
| V |
| n |
| V |


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:阅读理解
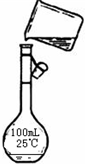 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):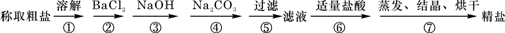
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室要配制0.5mol/L的NaOH溶液100mL,则:
实验室要配制0.5mol/L的NaOH溶液100mL,则:查看答案和解析>>
科目:高中化学 来源: 题型:
 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)| ①溶解 |
| ②BaCl2 |
| ③NaOH |
| ④Na2CO3 |
| ⑤过滤 |
| ⑥适量盐酸 |
| ⑦结晶、烘干 |
查看答案和解析>>
科目:高中化学 来源: 题型:
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备粗盐的实验方法,步骤如下(用于沉淀的试剂稍过量):称
![]()
|
![]() 取粗盐→
取粗盐→
![]()
![]()
![]() (1)判断BaCl2已过量的方法是:
(1)判断BaCl2已过量的方法是:
![]() _______________________________________________ _____
_______________________________________________ _____
![]()
![]() (2)过滤所必需的玻璃仪器是
(2)过滤所必需的玻璃仪器是
![]() _______________________________________
_______________________________________
![]() (3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是:______________________________________ ___
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是:______________________________________ ___
![]()
![]()
![]()
![]()

![]()
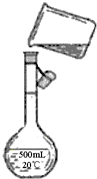
![]() (4)为检验精盐纯度,需要配制150mL0.2mol?L-1NaCl(精盐)溶液,如图所示是该同学转移溶液的示意图,图中的错误是__________________ _____ _
(4)为检验精盐纯度,需要配制150mL0.2mol?L-1NaCl(精盐)溶液,如图所示是该同学转移溶液的示意图,图中的错误是__________________ _____ _
![]()
![]()
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com