
【题目】雾霾中对人伤害最大的是PM2.5,即空气动力学直径小于2.5微米的粒子。分散质粒子直径约为2.5微米的分散系与下列哪种分散系最为接近
A.溶液 B.胶体 C.浊液 D.气溶胶
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好呈中性Ba2++OH-+H++SO42-=BaSO4↓+2H2O
B. NH4HCO3溶液中加入过量NaOH稀溶液: NH4+ + OH- = NH3 + H2O
C. 向醋酸溶液中通入氨气:H+ + OH- = H2O
D. 碳酸钙溶于稀硝酸: CaCO3 + 2H+ = Ca2+ + CO2 + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 硅酸钠可以作为粘合剂和防火材料
B. 溶液、胶体、浊液都属于分散系,且均为液态
C. 人体缺碘会引起甲状腺肿大,碘元素还被誉为“智慧之花”
D. 通常所说的三大有机合成材料为:塑料、合成橡胶、合成纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物X能发生水解反应,水解产物为Y和Z。同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是( )
A. 乙酸丙酯 B. 甲酸乙酯
C. 乙酸甲酯 D. 乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2![]() 2NO+O2在恒容的密闭容器中进行,达到平衡状态的标志是( )
2NO+O2在恒容的密闭容器中进行,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①④⑥⑦ B.②③⑤⑦ C.①③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42ˉ。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2),设计了如图所示的流程图:
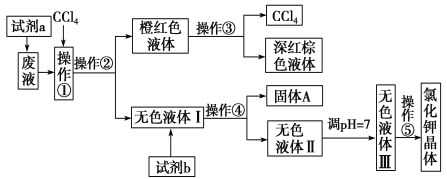
可供试剂a、试剂b(试剂b代表一组试剂)选择的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2溶液、酸性KMnO4溶液、稀盐酸。
请根据流程图,回答相关问题:
(1) 操作①②③④⑤的名称是_____________
①_______②________③________④________⑤________
(2) 除去无色液体Ⅰ中的Ca2+、Mg2+、SO42ˉ,选出试剂b所代表的试剂,按滴加顺序依次是________________(填化学式)。
(3)调节pH的目的是____________________,操作方法是_______________________。
(4)操作⑤中用到的瓷质仪器名称是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为
(1)4FeO·Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
(2)2Na2CrO4+H2SO4![]() Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法中正确的是
A.反应(1)和(2)均为氧化还原反应
B.反应(1)的氧化剂是O2,还原剂是Na2CO3
C.高温下,O2的氧化性大于Fe2O3小于Na2CrO4
D.生成13.1g的Na2Cr2O7时共转移0.35 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于胶体和溶液的区别,下列叙述中正确的是
A.溶液呈电中性,胶体带有电荷
B.溶液中溶质微粒的运动是有规律的,胶体中分散质微粒的运动是布朗运动
C.溶液中分散质微粒能透过滤纸,胶体中分散质微粒不能透过滤纸
D.溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现明亮的光路
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大。元素X是周期表中原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K位于ds区且原子的最外层电子数与X的相同。
请回答下列问题:(答题时,X、Y、Z、W、K用所对应的元素符号表示)
(1)Y、Z、W元素的第一电离能由大到小的顺序是 。
(2)K的电子排布式是 。
(3)Y、Z元素的某些氢化物的分子中均含有18个电子,则Y的这种氢化物的化学式是 ;Y、Z的这些氢化物的沸点相差较大的主要原因是 。
(4)若X、Y、W形成的某化合物(相对分子质量为46)呈酸性,则该化合物分子中Y原子轨道的杂化类型是 ;1 mol该分子中含有σ键的数目是 。
(5)Z、K两元素形成的某化合物的晶胞结构如右图所示,则该化合物的化学式是 ,Z原子的配位数是 。
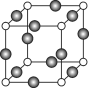
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com