
����Ŀ����֪����2H2(g)��O2(g)===2H2O(g)����H����483.6kJ/mol��
��H2(g)��S(g)===H2S(g)����H����20.1kJ/mol�������ж�һ����ȷ����(����)
A. �ɢ�����֪��2H2S(g)��O2(g)===2S(g)��2H2O(g)�� ��H����443.4kJ/mol
B. �ɢ�֪��������ȼ����Ϊ241.8kJ
C. ��Ӧ���е������仯������ͼ��ʾ
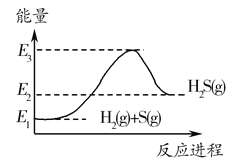
D. ����Ӧ���и��ù�̬������ȴ���20.1kJ
���𰸡�A
��������A����֪����2H2��g��+O2��g��=2H2O��g����H=-483.6kJ��mol��1����H2��g��+S��g��=H2S��g����H=-20.1kJ��mol��1���ɸ�˹���ɣ���-�ڵ�2H2S��g��+O2��g��=2S��g��+2H2O��g����H=-443.4 kJ��mol��1����A��ȷ��B��ȼ������1mol��ȼ����ȫȼ�������ȶ�������ų�������������ȼ�յ��ȶ�������ΪҺ̬ˮ����B����C����Ӧ��Ϊ���ȷ�Ӧ���������������С�ڷ�Ӧ�������������C����D����ӹ����Ϊ���壬Ҫ����������������Ӧ���и��ù�̬��1molS��s����ȫ��Ӧ���ų�������С��20.1kJ����D����ѡA��


 �ܿ�����ĩ��̾�ϵ�д�
�ܿ�����ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȫ�������ռ�ʹ������ʯͷֽ����������̼���Ϊ���ϣ��ڲ㣩������ϩ�ȸ߷��Ӳ���Ϊ���ϣ�˫��㣩�Ƴɵģ��й���ʯͷֽ����˵��������ǣ�������
A.����ȼ��B.�����ڱ���ɭ��C.���Ͳ���ˮD.������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ1�Dz��ֶ�����Ԫ�صij������ϼ���ԭ�������Ĺ�ϵͼ�� 
��1������Ԫ��F��ԭ�ӽṹʾ��ͼ ��
��2��������Ԫ����ѡȡ����Ԫ���γɼȺ����Ӽ��ֺ����ۼ��Ļ�����û�����ĵ���ʽΪ ��
��3����ЩԪ���У�����������Ӧ��ˮ������������ǿ�Ļ��������ʽΪ ��
��4��C��D��G��Ӧ�ļ����Ӱ뾶��С�����˳���� �� �������ӷ��Żش�
��5��ijͬѧ���ʵ��װ����ͼ2��֤��A��B��F�ķǽ�����ǿ����ϵ��
����Һa����Һb�ֱ�Ϊ �� ��
����Һc�е����ӷ�Ӧ����ʽΪ ��
�����ԭ�ӽṹ�ĽǶȽ��ͷǽ�����B��A��ԭ��
��6����1mol D2C2Ͷ��200mL 3mol/L EH3��Һ�У�
��ת�Ƶ��ӵ����ʵ���Ϊ ��
����һ����ѧ��Ӧ����ʽ��ʾ�÷�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����������Ļ�ѧ�仯����ȡ����Ӧ���ǣ� ��
A. ��FeBr3�������±���Һ�巴Ӧ B. �����������������±���������Ӧ
C. ��ϩ�ڿ�����ȼ�� D. �Ҵ���ͭ��������������������ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�ת���ڸ��������²���ʵ�ֵ��ǣ�������
A. ����NaCl��aq��![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
B. MgCl2��aq��![]() Mg��OH��2
Mg��OH��2![]() MgO
MgO
C. Al2O3![]() NaAlO2��aq��
NaAlO2��aq��![]() Al��OH��3
Al��OH��3
D. Fe2O3![]() FeCl3��aq��
FeCl3��aq��![]() ��ˮFeCl3
��ˮFeCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������й�����ʮ�˴�������ش���⣬��ͻ������̬�������ص�����ᷢչ����Ȼ����֮��ĺ�г��δ������Դ���ص�����Դ�ḻ����ʹ��ʱ�Ի�������Ⱦ����Ⱦ��С���ҿ�����������������δ������Դ������( )
����Ȼ�� ��̫���� �۷��� ��ʯ�� ��ú ���������� �ߺ��� ������
A.�٢ڢۢ�B.�ڢۢޢ�C.�٢ڢݢޢߢ�D.�ۢܢݢޢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.02 mol��L-1��Ba(OH)2��Һ100mL��0.02 mol��L-1NaHSO4��Һ100mL��ϣ���������Һ����仯�����Ϻ����Һ�� ��
A.pH��12B.���ʵ����ʵ���Ũ�ȣ�0.02 mol��L-1
C.pH��2D.��ˮ����IJ�����c(H��)��1.0��10-2mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ�����ǰѲ�1molij��ѧ�������յ��������ɸû�ѧ���ļ��ܡ����ܵĴ�С�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ��(��H)����ѧ��Ӧ����H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ

�������Ȼ�ѧ����ʽ����ȷ����(����)
A. 1/2A2(g)��1/2B2(g)��AB(g) ��H����91.5kJ��mol��1
B. A2(g)��B2(g)��2AB(g)����H����183kJ��mol��1
C. 2AB(g)��A2(g)��B2(g) ��H����183kJ��mol��1
D. 1/2A2(g)��1/2B2��AB(g) ��H����91.5kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��. ���з�Ӧ�����ӷ���ʽ�У���д��ȷ����
A. ʵ�����ô���ʯ��ϡ������ȡ������̼��2H+ + CO32- = CO2��+ H2O
B. ������Ͷ������������Һ�У� 2Al + 2OH- = 2AlO2- + H2��
C. ��������ˮ��Cl2 + H2O= 2H+ + Cl- + ClO-
D. ��������ˮ��Ӧ��2Na + 2H2O = 2Na+ + 2OH-+ H2��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com