
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:高一化学(通用各科奥林匹克ABC卷及解析) 题型:022
下表是元素周期表的一部分,列出11种元素在周期表中的位置,填写下空白

(1)这11种元素中化学性质最不活泼的是(写元素符号或化学式,以下同)________,金属性最强的是________.
(2)第三周期中,原子半径最小的是(稀有气体元素除外)________,单质氧化性最强的是________,离子还原性最强的是________.
(3)第二、三周期中,指定元素的单质是分子晶体的有________,熔点最高的是________,常温下能和水反应的有________.
(4)A、B、C、E四元素的最高价氧化物对应水化物,按碱性减弱酸性增强顺序排列为(写化学式)________.
(5)H、I两元素的最高价氧化物对应水化物的酸性________>________.I、J两元素的气态氢化物稳定性________>________.
(6)B和H、D和G所形成化合物的电子式分别为_________∶________,它们是以________键相结合,形成的晶体类型为________晶体.
(7)F和I、F和G所形成化合物的电子式分别为________、________,它们是以________键相结合.
查看答案和解析>>
科目:高中化学 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
下图是元素周期表的框架图,请根据下图回答问题.

(1)在上面元素周期表中全部是金属元素的区域为________.
(a)A (b)B (c)C (d)D
(2)在原子序数为1~18的元素范围中,用化学式填写:
与水反应最剧烈的金属元素是________,元素的气态氢化物最稳定的物质是________,元素的最高价氧化物所对应的碱的碱性最强的物质是________.
(3)用物质的名称填写:
硬度最大的单质是________,密度最小的气体单质是________.
(4)第3周期中,原子半径最大的非金属元素的原子是________,在上图中把该元素符号标出在合适的位置上.
查看答案和解析>>
科目:高中化学 来源:陕西省模拟题 题型:推断题
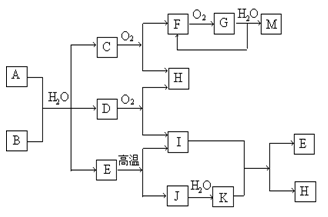
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com