
【题目】关于铝热反应,下列说法不正确的是( )
A.该反应是吸热反应
B.铝热剂是混合物
C.可以利用该反应焊接铁轨
D.该反应需在高温条件下进行
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向硝酸溶液中加入碳酸钠,有大量气泡产生 | 酸性:碳酸 > 硝酸 |
B、 | 向1mL 某溶液中,滴入2 mL 0.1 mol·L-1 NaOH溶液,加热,产生使湿润的红色石蕊试纸变蓝的气体 | 某溶液中含NH4+ |
C、 | 取5 mL 0.1 mol·L-1FeCl3溶液,滴加5滴0.1 mol·L-1KI溶液,振荡,再加入5 mL CCl4,振荡,静置,取上层液体,向取出来的溶液中滴加KSCN溶液,显血红色。 | KI和FeCl3反应有一定的限度 |
D、 | 加热使冰化成液态水 | 分子内H-O键发生断裂 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.若丙醇中的氧为188O,它与乙酸反应生成的酯的相对分子质量是104
B.用乙酰水杨酸![]() 与适量NaOH溶液反应制备
与适量NaOH溶液反应制备![]()
C.向柠檬醛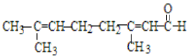 中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基
中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基
D.![]() 、
、![]() 、
、![]() 三种氨基酸脱水,最多可生成 6种二肽。
三种氨基酸脱水,最多可生成 6种二肽。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可充电电池的原理如图所示,已知a、b为惰性电极,溶液呈酸性。充电时右槽溶液颜色由绿色变为紫色。下列叙述正确的是

A. 放电时,H+从左槽迁移进右槽
B. 放电过程中,左槽溶液颜色由黄色变为蓝色
C. 充电时,b极接直流电源正极,a极接直流电源负极
D. 充电过程中,a极的电极反应式为:VO2++2H++e- = VO2++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组在通过反应Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O研究反应速率的影响因素后,对Na2S2O3产生了兴趣,查资料知Na2S2O3的名称为硫代硫酸钠,可视为一个S原子取代了Na2SO4中的一个O原子。该实验小组运用类比学习的思想预测了Na2S2O3的某些性质,并通过实验探究了自己的预测。
【提出假设】
(1)部分学生认为Na2S2O3与Na2SO4结构相似,化学性质也相似,因此室温时Na2S2O3溶液的pH____7(填“>”、“=”或“<”)。
(2)部分学生从S元素化合价推测Na2S2O3与Na2SO4性质相似,均具有较强的____。
【实验探究】取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写表中空格)。
实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
探究① | (3)____ | 溶液pH=8 | (4)____ |
探究② | 向新制氯水(pH<2)中滴加少量Na2S2O3溶液 | 氯水颜色变浅 | (5)____ |
【实验结论】
(6)探究①__________。
(7)探究②__________。
【问题讨论】
(8)甲同学向“探究②”反应后的溶液中滴加硝酸银溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。你认为该方案是否正确并说明理由___________。
(9)请你重新设计一个实验方案,证明Na2S2O3被氯水氧化。你的方案是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国化学家凯库勒认为苯分子的结构中,碳碳间以单、双键交替结合而成环状。 为了评价凯库勒的观点,某学生设计了以下实验方案:

实验操作:
①按上图所示的装置图连接好各仪器;
②检验装置的气密性;
③在 A 中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开 K1、K2止水夹,关闭 K3 止水夹;
④待烧瓶 C 中气体收集满后,将导管 b 的下端插入烧杯里的水中,关闭 K2,打开 K3,挤 压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题:
(1)实验室可用 MnO2、NaBr 和浓硫酸混合共热制取单质溴,其中 MnO2 作氧化剂。写 出该反应的化学方程式:____。
(2)简述在实验操作步骤②中检验装置气密性的方法:_____________________;在实验过程中观察到装置 A 中有微沸现象,原因是_______________________。
(3)当 C 中观察到____,可证明凯库勒观点是错误的,以下 还可证明凯库勒观点错误的事实是________。
①6 个 C-H 键的长度相等
②6个碳碳键的长度都相等
③苯的一氯代物只有一种结构
④苯的邻二氯代物只有一种结构
⑤苯不能使酸性高锰酸钾溶液褪色
⑥苯不能使溴的四氯化碳溶液因加成而褪色
A.①②⑤⑥ B.②④⑤⑥ C.全部 D.①②③④⑤
(4)查阅文献:苯与液溴在 FeBr3 催化下的反应机理共分三步:
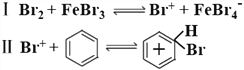
请完成第三步反应:Ⅲ____。
(5)将装置 A 内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯:
①用蒸馏水洗涤,振荡,分液;②用 5%的 NaOH 溶液洗涤,振荡,分液;③用蒸馏水洗 涤,振荡,分液;④加人无水氯化钙干燥;⑤____(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关除杂的实验操作合理的是( )
A.除去二氧化碳中混有的少量一氧化碳:通入适量氧气后点燃
B.除去氧气中少量的氮气:使气体通过炽热的铜粉
C.除去铜粉中少量的碳酸钙:用稀盐酸溶解后过滤
D.除去氯化钠固体中少量的纯碱:加入足量氯化钙溶液,过滤、蒸发、结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素的电负性用来描述不同元素的原子对键合电子吸引力的大小。电负性应用:
判断元素的金属性和非金属性的强弱。下表列出了同周期的几种短周期元素的部分性质
请回答下列问题:

(l)写出D元素的离子结构示意图_______________;
(2)X的值应为____(填字母);
A.3.6 B.3.1 C.1.4 D.2.1
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系:________________________________;
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是:__________________
(用化学式表示)
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com