
| A、铜 | B、银 | C、铝 | D、镁 |
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
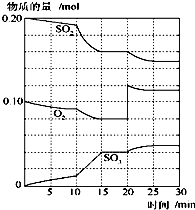 (1)在一定温度和压强下,有如下反应:2SO2(g)+O2(g) 2SO3(g),将1.6molSO2和0.8mol的O2放入一体积可变的密闭容器中,测得容器的起始容积为100L.经一段时间后,反应达到平衡,测得混合气体的密度为1.6g?L-1.请回答下列问题:
(1)在一定温度和压强下,有如下反应:2SO2(g)+O2(g) 2SO3(g),将1.6molSO2和0.8mol的O2放入一体积可变的密闭容器中,测得容器的起始容积为100L.经一段时间后,反应达到平衡,测得混合气体的密度为1.6g?L-1.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 配料表 | 精制海盐、碘酸钾 |
| 含碘量 | 20~40mg/kg |
| 卫生许可证号 | ××卫碘字(1999)第001号 |
| 分装日期 | 见封底 |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 防治禽流感病毒目前人类面临的一个重大课题.八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如下图所示,下列关于莽草酸的说法正确的是( )
防治禽流感病毒目前人类面临的一个重大课题.八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如下图所示,下列关于莽草酸的说法正确的是( )| A、莽草酸的分子之间可能发生酯化反应 |
| B、莽草酸的分子式为C7H4O5 |
| C、莽草酸中含有苯环 |
| D、莽草酸能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀硝酸是弱酸,浓硝酸是强酸 |
| B、铜与浓、稀硝酸反应都生成NO2 |
| C、浓、稀硝酸在空气中都产生“发烟”现象 |
| D、浓、稀硝酸都是强氧化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com