
 某实验小组用MnO2与浓盐酸混合加热制取Cl2,并将制得的氯气与潮湿的Ca(OH)2固体反应制取少量漂白粉.实验装置如图:回答下列问题.
某实验小组用MnO2与浓盐酸混合加热制取Cl2,并将制得的氯气与潮湿的Ca(OH)2固体反应制取少量漂白粉.实验装置如图:回答下列问题.
| ||
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾和FeCl3可作净水剂 |
| B、为保存FeCl3溶液,要在溶液中加少量盐酸 |
| C、用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 |
| D、氢氟酸用塑料试剂瓶保存而不用玻璃试剂瓶保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸溶液的pH大于盐酸 |
| B、醋酸溶液的pH小于盐酸 |
| C、与NaOH完全中和时,醋酸消耗的NaOH多于盐酸 |
| D、分别用水稀释相同倍数后,所得溶液中:n (Cl-)=n (CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
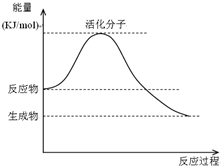 (1)如图是某化学反应中的能量变化图.
(1)如图是某化学反应中的能量变化图.查看答案和解析>>
科目:高中化学 来源: 题型:
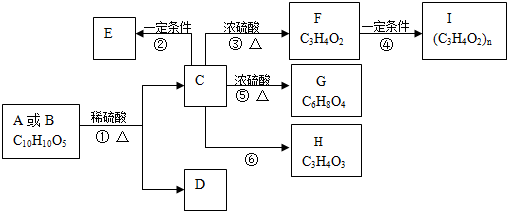
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com