
| 3 | 2 |
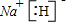 ,
,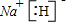 ;
;| 3 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012-2013学年安徽省池州市高三上学期期末统考理综化学试卷(解析版) 题型:填空题
现有五种短周期主族元素A、B、C、 D、E,其原子序数依次增大。A原子约占宇宙中原子总数的88.6%,A+又称为质子:B是形成化合物种类最多的元素,C元素的最简单的氢化物Y的水溶液显碱性.E是短周期元素中电负性最小的元素。A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。试回答下列问题:
(1)写出A、E两元素形成的原子个数比为1:1的化合物的电子式____。
(2)向氯化亚铁溶液滴加过量的E的最高价氧化物对应水化物的溶液,现象是____。
(3)Y溶液显碱性的原因是(用一个离子方程式表示)____。
(4)检验汽车尾气中含有的化合物BD的方法是:向酸性PdC12溶液中通A汽车尾气,若生成黑色沉淀(Pd),证明汽车尾气中含有BD。写出反应的离子方程式____。
(5)下列有关物质性质的比较中.不正确的是 。
a.热稳定性:H2S>SiH4 b.离子半径:Na+>S2-
c.第一电离能N>O d.元素电负性:C>H
(6)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H=-192.9kJ/mol
由上述方程式可知.CH3OH的燃烧热____(填“大于”、“等于”或小于”)192.9kJ/mol。已知水的气化热为44 kJ/mol.则表示氢气燃烧热的热化学方程式为____。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Z、W、R最高价氧化物对应水化物的酸性强弱顺序是R>W>Z |
| B.Y的氢化物比R的氢化物稳定,Y的氢化物的熔沸点比R的氢化物的熔沸点低 |
| C.Y分别与Z、W、R以两种元素组成的常见化合物共有5种 |
| D.X与Y形成的两种化合物中,阴、阳离子的个数比均为1:2 |
查看答案和解析>>
科目:高中化学 来源:2013年高考化学备考复习卷C4:物质结构和元素周期律(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com