
分析 设此烷烃的分子式为CnH2n+2,根据燃烧的通式CnH2n+2+$\frac{3n+1}{2}$O2 $\stackrel{点燃}{→}$ n CO2+(n+1)H2O 计算.
解答 解:设此烷烃的分子式为CnH2n+2,
CnH2n+2+$\frac{3n+1}{2}$O2 $\stackrel{点燃}{→}$ n CO2+(n+1)H2O.
14n+2 n n+1
5.8g 0.4mol 0.5mol
解得n=4,则
(1)烷烃的相对分子质量为12×4+2×4+2=58,
故答案为:58;
(2)n=4,此烷烃的化学式为C4H10,
故答案为:C4H10;
(3)该烷烃的分子式为C4H10,是丁烷,丁烷存在正丁烷和异丁烷两种同分异构体,其可能结构及名称为:正丁烷:CH3CH2CH3CH3,异丁烷:CH3CH(CH3)2(也就是2-甲基丙烷),
故答案为:CH3CH2CH3CH3、CH3CH(CH3)2.
点评 本题考查了有机物分子式、结构简式的确定及有机物命名,题目难度不大,明确烷烃的组成、烷烃的命名原则为解答关键,试题培养了学生的分析能力及灵活应用基础知识的能力.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:实验题
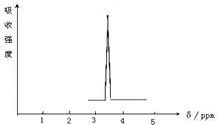 按要求完成下列问题:
按要求完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
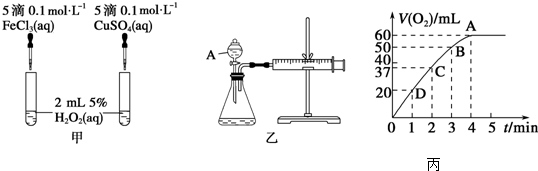
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
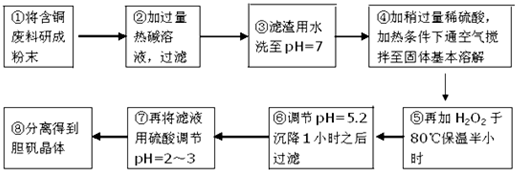
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 | Fe(OH)2 |
| pH | 5.2 | 3.1 | 6.7 | 9.4 | 9.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
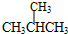 和
和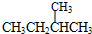 ;⑧
;⑧ 和
和 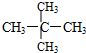 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl晶体中每个钠离子与周围6个氯离子形成6个离子键 | |
| B. | 前四周期元素的原子中,未成对电子数最多的是Mn | |
| C. | 金属导电的原因是在外电场作用下金属产生自由电子,电子定向运动 | |
| D. | 岩浆冷却过程中,晶格能高的矿物晶体先结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol任何气体都含有相同的原子数 | |
| B. | 在100℃、1×104Pa时,1mol O2中约含有6.02×1023个O2分子 | |
| C. | 含有阿伏加德罗常数个水分子的水(4℃)其体积为18mL(ρ=1g/cm3) | |
| D. | 两种物质完全反应时,它们的物质的量一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S气体能用浓硫酸进行干燥(浓硫酸的吸水性) | |
| B. | 铜与浓硝酸制备NO2气体(浓硝酸的强氧化性、酸性) | |
| C. | SO2的水溶液能够使品红溶液褪色(H2SO3的强氧化性) | |
| D. | 可口可乐瓶盖打开后,有大量气体逸出(H2CO3的挥发性) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com