
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。某同学设计了如下实验方案并验证产物、探究反应原理。
(1)提出假设
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为 。
猜测2:白色不溶物可能为MgCO3。
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3·yMg(OH)2]。
(2)设计定性实验确定产物并验证猜测:
|
实验序号 |
实验 |
实验现象 |
结论 |
|
实验Ⅱ |
将实验I中收集到的气体点燃 |
能安静燃烧、产生淡蓝色火焰 |
气体成分为 _ _ |
|
实验Ⅲ |
取实验I中的白色不溶物,洗涤, 加入足量‚ |
ƒ |
白色不溶物可能含有MgCO3 |
|
实验Ⅳ |
取实验I中的澄清液,向其中加入少量CaCl2稀溶液 |
产生白色沉淀 |
溶液中存在 ④ 离子 |
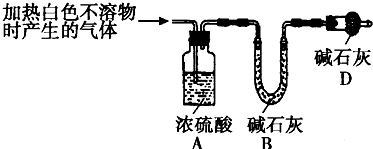
(3)为进一步确定实验I的产物,设计定量实验方案,如图所示:

称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验前后装置A增重1.8 g,装置B增重8.8 g,试确定白色不溶物的化学式 。
(4)用必要的语言文字叙述并结合方程式说明为什么碳酸氢钠溶液能和镁反应生成氢气?
(1)猜测1:Mg(OH)2 (2分) (2)①氢气 ②稀盐酸(合理均可) ③ 产生气泡,沉淀全部溶解 ④CO32-(各1分)(3) 2MgCO3·Mg(OH)2 或 Mg(OH)2·2MgCO3 或 Mg3(OH)2(CO3)2
(4)NaHCO3溶液中存在如下平衡:HCO3-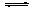 H+
+CO32-、H2O
H+
+CO32-、H2O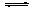 H++OH-;Mg和H+反应生成H2和Mg2+,Mg2+跟OH-、CO32-生成难溶物Mg(OH)2·2MgCO3,则H+、OH-、CO32-的浓度均降低,促使上述两平衡均向右移动。故Mg和饱和NaHCO3溶液反应产生大量气体H2。
H++OH-;Mg和H+反应生成H2和Mg2+,Mg2+跟OH-、CO32-生成难溶物Mg(OH)2·2MgCO3,则H+、OH-、CO32-的浓度均降低,促使上述两平衡均向右移动。故Mg和饱和NaHCO3溶液反应产生大量气体H2。
【解析】
试题分析:(1)根据猜测2和3可判断,猜测1应该是白色不溶物可能为Mg(OH)2。
(2)①能安静燃烧、产生淡蓝色火焰,这说明该气体应该是氢气。
②碳酸镁能溶于酸中放出CO2气体,所以可以通过检验CO2来验证是否含有碳酸镁,即试剂②可以是稀盐酸。如果产生气泡,沉淀全部溶解,则说明只含有的是碳酸镁。
③如果取实验I中的澄清液,向其中加入少量CaCl2稀溶液,能产生白色沉淀,这说明该白色沉淀应该是碳酸钙,即溶液中含有CO32-。
(3)A中含有浓硫酸,吸收的是水蒸气,即水蒸气的质量是1.8g,物质的量是0.1mol。碱石灰吸收的是CO2,即CO2的质量是8.8g,物质的量是0.2mol,这说明该白色沉淀是氢氧化镁和碳酸镁饿混合物,且二者的物质的量之比是1:2,则化学式为2MgCO3·Mg(OH)2 或 Mg(OH)2·2MgCO3或Mg3(OH)2(CO3)2。
(4)NaHCO3溶液中存在如下平衡:HCO3-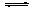 H+
+CO32-、H2O
H+
+CO32-、H2O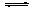 H++OH-;Mg和H+反应生成H2和Mg2+,Mg2+跟OH-、CO32-生成难溶物Mg(OH)2·2MgCO3,则H+、OH-、CO32-的浓度均降低,促使上述两平衡均向右移动。故Mg和饱和NaHCO3溶液反应产生大量气体H2。
H++OH-;Mg和H+反应生成H2和Mg2+,Mg2+跟OH-、CO32-生成难溶物Mg(OH)2·2MgCO3,则H+、OH-、CO32-的浓度均降低,促使上述两平衡均向右移动。故Mg和饱和NaHCO3溶液反应产生大量气体H2。
考点:考查镁和饱和碳酸氢钠溶液反应的实验探究
点评:该题是高考中的常见题型,试题综合性强,对学生的思维能力要求高。该题以探究镁和饱和碳酸氢钠溶液反应为载体,重点考查学生的化学实验基本操作、实验分析与评价、定量计算等,有利于培养学生的逻辑思维能力和规范的实验设计能力。该类试题综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:阅读理解
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | ①气体成分为 氢气 氢气 |
| 实验Ⅲ | ②取实验Ⅰ中的白色不溶物,洗涤,加入足量 稀盐酸 稀盐酸 |
③ 产生气泡沉淀全部溶解 产生气泡沉淀全部溶解 |
白色不溶物可能含有MgCO3 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀 | ④溶液中存在 CO32- CO32- |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体成为 ①氢气 ①氢气 |
| 实验Ⅲ | 取实验Ⅰ中的白色不溶物,洗涤, 加入足量 ②稀盐酸 ②稀盐酸 |
③产生气体沉淀全部溶解 ③产生气体沉淀全部溶解 |
白色不溶物可能是MgCO3 |
| 实验Ⅳ | 取实验Ⅰ中的澄清溶液, 向其中加入少量稀CaCl2溶液 |
产生白色沉淀 | 溶液中存在 ④CO32- ④CO32- |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年安徽省高三上学期期中考试化学试卷(解析版) 题型:实验题
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。某同学通过如下实验探究反应原理并验证产物。
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛适量滴有酚酞的饱和碳酸氢钠溶液的烧杯中,迅速反应,产生大量气泡和白色不溶物,溶液的浅红色加深。
(1)该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为
猜测2:白色不溶物可能为MgCO3
猜测3:白色不溶物可能为碱式碳酸镁[yMg(OH)2•xMgCO3]
(2)为了确定产物,进行以下定性实验:
|
实验序号 |
实 验 |
实验现象 |
结 论 |
|
实验Ⅱ |
将实验I中收集到的气体点燃 |
安静燃烧, 火焰呈淡蓝色 |
气体成分为 ① |
|
实验Ⅲ |
将实验I中的白色不溶物滤出、洗涤,取少量加入足量 ② |
③ |
白色不溶物中含有MgCO3 |
|
实验Ⅳ |
取实验Ⅲ中的滤液,向其中加入适 量 ④ 稀溶液 |
产生白色沉淀,溶液红色变浅 |
溶液中存在CO32- 离子 |
实验Ⅲ中洗涤的操作方法是 。
(3)为进一步确定实验I的白色不溶物的成分,进行以下定量实验,装置如图所示:

称取干燥、纯净的白色不溶物 4.52 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验后装置A增重0.36 g,装置B增重1.76 g。
装置C的作用是 ;
白色不溶物的化学式为 。
(4)写出镁与饱和碳酸氢钠溶液反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市海淀区高三上学期期末考试化学试卷(解析版) 题型:实验题
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。某同学设计了如下实验方案并验证产物、探究反应原理。
(1)提出假设
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为 。
猜测2:白色不溶物可能为MgCO3。
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3·yMg(OH)2]。
(2)设计定性实验确定产物并验证猜测:
|
实验序号 |
实验 |
实验现象 |
结论 |
|
实验Ⅱ |
将实验I中收集到的气体点燃 |
能安静燃烧、产生淡蓝色火焰 |
气体成分为______ |
|
实验Ⅲ |
取实验I中的白色不溶物,洗涤,加入足量 ‚ |
ƒ |
白色不溶物可能含有MgCO3 |
|
实验Ⅳ |
取实验I中的澄清液,向其中加入少量CaCl2稀溶液 |
产生白色沉淀 |
溶液中存在 ④ 离子 |
(3)为进一步确定实验I的产物,设计定量实验方案,如图所示:

称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验前后装置A增重1.8 g,装置B增重8.8 g,试确定白色不溶物的化学式 。
(4)请结合化学用语和化学平衡移动原理解释Mg和NaHCO3溶液反应产生大量气泡的原因_________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省梅州市高三总复习质检二理综化学试卷(解析版) 题型:实验题
某兴趣小组根据镁与沸水的反应推测镁也能与饱和碳酸氢钠溶液反应。资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。该兴趣小组设计了如下实验方案并验证产物、探究反应原理。
实验1:用砂纸擦去镁条表面氧化膜,将其放人盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
(1)提出假设
该同学对反应中产生的白色不溶物作出如下假设:
假设1:可能为 。
假设2:可能为MgCO3。
假设3:可能是碱式碳酸镁[xMgCO3·yMg(OH)2]
(2)设计定性实验确定产物并验证猜测:
|
实验序号 |
实验 |
预期现象和结论 |
|
实验II |
将实验I中收集到的气体点燃 |
|
|
实验III |
取实验I中的白色不溶物,洗涤,加入足量 |
; 白色不溶物可能含有MgCO3 |
|
实验IV |
取实验I中的澄清液,向其中加入少量CaCl2稀溶液 |
产生白色沉淀;溶液中存在 离子 |
(3)设计定量实验确定实验I的产物:称取实验I中所得干燥、纯净的白色不溶物31.0 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入盛有足量浓硫酸的洗气瓶A、盛有足量碱石灰的干燥管B和盛有足量碱石灰的干燥管C中。实验前后装置A增重1.8 g,装置B增重13.2 g,试确定白色不溶物的化学式 。
(4)请结合化学用语和化学平衡移动原理解释Mg和NaHCO3溶液反应产生大量气泡的原因 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com